Бериллий и магний.
!!!!
карбид бериллия разлагается водой с выделением ацетилена. Он является, следовательно, типичным ацетилидом.
69) Из карбидов магния — MgC2 и Mg4C3 — первый удобно получать нагреванием порошкообразного Mg до 500 °С в токе этана, второй — до 600 °С в токе пентана. Оба карбида являются эндотермичными соединениями с теплотами образования из элементов соответственно -21 и -18 ккал/моль. Водой MgC2 разлагается с выделением ацетилена, а Mg4C3 — аллилена (СН3-СºСН) и аллена (H2C=C=CH2). Выше 550 °С MgC2 распадается на углерод и Mg2C3, который выше 750 °С разлагается на элементы. Последний карбид является единственным соединением этого класса, содержащим в своей структуре анионы [С=С=С]4+.
70) Из силицидов магния известны Mg2Si (т. пл. 1100 °С) и Mg!!!!Si!!!!. В отличие от MgC2, теплота образования Mg2Si из элементов положительна (19 ккал/моль). Бериллий сплавляется с кремнием, но определённых соединений с ним не образует. Из аналогов силицида магния были получены !!!!MgaSn (т. пл. 780 °С) и Mg2Pb (теплоты образования из элементов соответственно 18 и 13 ккал/моль). Последнее соединение бурно реагирует с водой.
71) Основными типами боридов являются, по-видимому, для бериллия !!!!, а для магния — !!!!. Наиболее характерны из них медно-красный Ве2В и черный MgB2. Бориды с относительно малым содержанием бора кислотами (или даже водой) разлагаются, с большим — не разлагаются.
72) Для бериллия довольно характерно образование с некоторыми другими металлами соединений (“бериллидов”), обычно содержащих относительно много атомов Be. Примерами могут служить !!!!. Последнее из этих соединений находит использование в качестве источника нейтронов.
73) Производные одновалентных бериллия и магния не получены. В качестве промежуточных продуктов ионы Be+ и Mg+ образуются, по-видимому, при анодном окислении этих металлов. С равновесием по схеме !!!! связана, вероятно, частичная (порядка одного атома на 100 молекул) растворимость магния в расплаве его хлорида.
Существование BeF и Be!!!! при высоких температурах установлено для систем ВеГ2(г) + Ве(ж) Û 2 ВеГ(г). Теплота образования газообразного BeF из элементов положительна (40 ккал/моль) а BeCl — отрицательна (-4 ккал/моль). Теоретические расчеты показывают, что галогениды ЭГ не должны устойчиво существовать при обычных условиях (так как их дисмутация на ЭГ2 и Э энергетически выгодна). Напротив, при очень высоких температурах одновалентное состояние становится устойчивее двухвалентного, как то видно из показанных на рис. результатов теоретического расчета равновесий термической диссоциации хлоридов магния.
74) Нульвалентное состояние Bе и Mg представлено их малоизученными дипиридильными производными - Э(Dipу)2. Они представляют собой тёмноокрашенные твердые вещества, растворы которых в тетрагидрофуране (при отсутствии даже следов кислорода) имеют зеленый (Be) или красный (Mg) цвет.
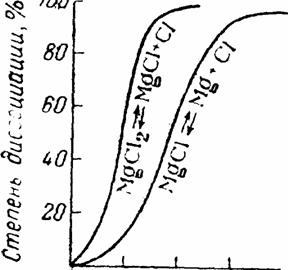
Рис. XII-6. Термическая
диссоциация магния.
заметным лишь немного выше 100, для MgCO3 — около 500 °С. CO2 MgO (MgO)
MgCO3
MgCO3 + H2O + CO2 = Mg(HCO3)2
CO2
Be (NH42CO3 M2[Be(CO3)2] K2[Mg(CO3)2]·4H2O KH[Mg(CO3)2]·4H2O Ca[Mg(CO3)2]. (NH4)2CO3
Mg(ClO4)2·6H2O Mg(ClO4)2
Be(ClO4)2·4H2O [Be(OH2)4](ClO4)2
Be(CH3COO)2 BeCl2
Mg(CH3COO)2·4H2O Mg(CH3COO)2 O®Mg
BeC2O4·3H2O BeSO4 Be[Be(C2O4)2]·6H2O BeC2O4 Na2[Be(C2O4)2]·H2O
47
33-74
По химическому характеру оба рассматриваемых элемента, в общем похожи друг на друга. Основные различия между ними связаны со значительным увеличением ионного радиуса при переходе от Be2+ (34 пм) к Mg2+ (78 пм).
Смотрите также
Предисловие редактора перевода
Historia est magistra vitae: История — учитель жизни.
По-разному реализовывали этот древний латинский завет историки науки. Иногда
история науки использовалась в качестве инструмента оценки нау ...
Обсуждение результатов эксперимента
В эксперименте принимали
участие ученики 9 классов МОУ СОШ-гимназии № 1 г. Нальчик (выборочная
совокупность составляла 45 школьников).
В
экспериментальных классах при раскрытии темы « ...
Железо и его роль
Железо -
(лат. Ferrum), Fe (читается «феррум»), химический элемент, атомный номер 26,
атомная масса 55,847. Происхождение как латинского, так и русского названий
элемента однозначно не уста ...
