Гидрофобная хроматография белков
Как известно, поверхность белковой глобулы богата гидрофильными аминокислотами, но в то же время содержит немало (до половины от их общего содержания) гидрофобных остатков, нередко образующих скопления ("гроздья"). Такие гидрофобные зоны, развитые в большей или меньшей степени, представляют характерную особенность структуры каждого белка, на чем и основан метод гидрофобной хроматографии. Соответствующие сорбенты синтезируют, включая гидрофобные группировки в гидрофильную матрицу, например в поперечно-сшитую агарозу — сефарозу. По такому принципу построены, в частности, октил- и фенилсефароза:
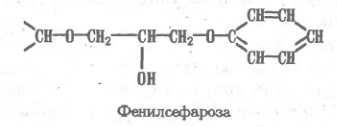
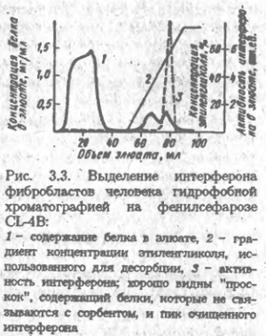 |
Сходным образом действуют сорбенты, полученные присоединением к макропористому кремнезему гидрофобных алкильных радикалов
различной длины. Они, будучи жесткими, особенно подходят для работы при повышенном давлении в условиях высокоэффективной жидкостной хроматографии (ВЭЖХ, англ. HPLC). Те из них, которые содержат длинные —![]() -уг леводородные цепи, малопригодны для разделения белков из-за слишком сильного, нередко необратимого связывания, ио могут применяться для хроматографии пептидов. Лучшие результаты дает хроматография белков на сорбентах, содержащих более короткие — С4 —
-уг леводородные цепи, малопригодны для разделения белков из-за слишком сильного, нередко необратимого связывания, ио могут применяться для хроматографии пептидов. Лучшие результаты дает хроматография белков на сорбентах, содержащих более короткие — С4 —![]() углеводородные цепи.
углеводородные цепи.
Нередко гидрофобная хроматография сочетается с другими эффектами. Например, присоединение к активированной бромцианом сефарозе диаминов различной длины дает сорбенты, в которых содержатся гидрофобные углеводородные цепочки наряду с двумя катионными группами. Объединение черт гидрофобного сорбента и анионита в одном хроматографическом материале обогащает его.
Описанный выше способ проведения хроматографии на гидрофобном сорбенте — далеко не единственно возможный. Для сорбции белков не обязательно введение в раствор повышенных концентрация соли, а для элюцни можно применять добавление органических растворителей, сдвиг рН. В некоторых случаях, когда связывание белка основано на сочетании гидрофобных и ионных взаимодействий, хорошие результаты дает элюция растворами солей. Отметим также, что признаки гидрофобной хроматографии встречаются и в других приемах разделения белков, в особенности в аффинной хроматографии.
Смотрите также
Третий закон термодинамики
Понятие химического сродства. Известно, что многие
вещества реагируют друг с другом легко и быстро, другие вещества реагируют с
трудом, а третьи – не реагируют. Исходя из этого, вывели предположени ...
Кремний, полученный с использованием геттерирования расплава
В бездефектной технологии
изготовления ИС для уменьшения влияния термодефектов используются методы
пассивного геттерирования примесей в пластинах. К таким методам относятся
"внешнее г ...
Зависимость точности визуального тест-определения нитрит-иона на основе пенополиуретана от способа построения цветовой шкалы
Определение
микроколичеств нитрит-ионов в водах, почвах и пищевых продуктах относится к
числу важных задач в связи с широким и зачастую неумеренным применением в
качестве удобрений нитратов ...
