Основность аминов в газовой фазе
Из рассмотрения данных по основности аминов в растворах следует, что она существенно зависит от электронных и пространственных факторов структуры и сольватации исследуемых соединений. Несмотря на отмеченные успехи при выявлении отдельных зависимостей между основностью и указанными эффектами, до сих нет единого количественного подхода к решению проблемы в целом. Казалось бы, что для оценки влияния строения аминов на их основность наиболее удобными есть соответствующие характеристикистики в газовой фазе, в которой, естественно, сольватационные эффекты отсутствуют. С этой точки зрения большой интерес представляет серия появившихся в последнее время работ (в том числе и обзорных [3, 6, 7, 21,137—140]), в которых обобщены результаты масс-спектрометрических методов, в которых определялись энергии перехода протона между стандартным и рассматриваемым (В) аминами в газовой фазе:
![]() В0Н+ + В В0 + ВН + (1)
В0Н+ + В В0 + ВН + (1)
Наличие свободной энергии этого процесса характеризует основность амина В относительно стандарта В0. Абсолютная основность (В0), равная отрицательной свободной энергии (DG0) процесса (8), может быть рассчитана, если известно соответствующее
В + Н+=ВН+ (2)
абсолютное значение для стандартного основания. Энтальпия (DH0) процесса (8), взятая с обратным знаком, характеризует сродство аминов к протону (РА) и легко рассчитывается, так как для прото-нирования аммиака, обычно принимаемого за стандарт, она определена независимыми методами [139, 143, 148, 149, 150]. Абсолютные значения 0В и РА* зависят от выбранного стандарта и абсолютной величины РА для него (например, для аммиака значение РА изменяется достаточно широко: 200,7 [139]; 201,4 [151]; 202,3 ± 2,0 [152]; 207 ± 3 [143, 148, 150, 153], 211,3 [149]; 214,4 [45]). Поэтому для выяснения количественных закономерностей влияния структуры аминов на их основность в газовой фазе лучше всего пользоваться величинами DGB (или — dRDG0 [3,7, 47]), когда за стандарт выбран аммиак**.
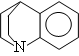
В табл.1 приведены величины DGB известного к началу 1977 г. ряда аминосоединений. Сопоставление этих данных показывает, что поведение различных аминов как оснований в газовой фазе резко отличается от такового в конденсированных средах. Например, анилин (табл. 1, № 31) в газовой фазе оказался на 6,7 ккал/моль (или почти на 5 ед. рКа) более основным, чем аммиак (№ 1), в то время как в воде, нитрометане и ацетонитриле (см. выше) наблюдается противоположная ситуация. Аналогичная картина имеет место и для пиридина, который в конденсированной фазе примерно на 4 ед. рКа менее основен, а в газовой фазе (№ 80) на 16 ккал/моль (или ~ на 12 ед. рКа) более основен, чем аммиак; для ацетамида (№ 32), который в воде ~ на 10 ед. рКа менее основен по сравнению с аммиаком, а в газовой фазе практически равен ему; для пиррола (№ 54) и некоторых других аминосоединений.
Таблица 1. Значения основностиа аминосоеденений в газовой фазеб относительно аммиака
|
Номер |
Амин |
DGBг) | ||||
|
1 |
NH3 |
0,0 | ||||
|
2 |
CH3NH2 |
9,1 | ||||
|
3 |
C2H5NH2 |
11,8 | ||||
|
4 |
n-C3H7NH2 |
13,0 | ||||
|
5 |
i-C3H7NH2 |
14,1 | ||||
|
6 |
n-C4H9NH2 |
13,5 | ||||
|
7 |
i-C4H9NH2 |
14,0 | ||||
|
8 |
s-C4H9NH2 |
15,2 | ||||
|
9 |
t-C4H9NH2 |
16,1 | ||||
|
10 |
n-C5H11NH2 |
13,4д) | ||||
|
11 |
t-C5H11NH2 |
17,4 | ||||
|
12 |
n-C6H13NH2 |
13,5д) | ||||
|
13 |
n-C7H15NH2 |
13,6д) | ||||
|
14 |
c-C6H11NH2 |
16,3 | ||||
|
15 |
NH2-NH2 |
3,8 | ||||
|
16 |
NH2(CH2)2NH2 |
19,0д) | ||||
|
17 |
NH2(CH2)3NH2 |
24,5д) | ||||
|
18 |
NH2(CH2)4NH2 |
27,1д) | ||||
|
19 |
NH2(CH2)5NH2 |
25,4д) | ||||
|
20 |
NH2(CH2)6NH2 |
25,4д) | ||||
|
21 |
NH2(CH2)7NH2 |
25,2е) | ||||
|
22 |
CH3O(CH2)2NH2 |
14,7д) | ||||
|
23 |
H2C=CH-CH2NH2 |
11,3 | ||||
|
HCºC-CH2NH2 |
6,7 | ||||
|
25 |
NCCH2CH2NH2 |
3,0 | ||||
|
26 |
CF3(CH2)3NH2 |
10,1 | ||||
|
27 |
FCH2CH2NH2 |
8,0 | ||||
|
28 |
CF3(CH2)2NH2 |
6,7 | ||||
|
29 |
F2CHCH2NH2 |
4,0 | ||||
|
30 |
CF3CH2NH2 |
-1,4 | ||||
|
31 |
|
6,8 | ||||
|
32 |
CH3CONH2 |
0,2ж) | ||||
|
33 |
HCONH2 |
-7,1з) | ||||
|
34 |
(CH3)2NH |
15,5 | ||||
|
35 |
CH3NHC2H5 |
17,9 | ||||
|
36 |
(C2H5)2NH |
20,2 | ||||
|
37 |
(n-C3H7)2NH |
22,2 | ||||
|
38 |
(i-C3H7)2NH |
23,9 | ||||
|
39 |
(n-C4H9)2NH |
23,1 | ||||
|
40 |
(i-C4H9)2NH |
23,6 | ||||
|
41 |
(s-C4H9)2NH |
25,8 | ||||
|
42 |
|
11,2 | ||||
|
43 |
|
18,0 | ||||
|
44 |
|
20,1 | ||||
|
45 |
|
21,2 | ||||
|
46 |
|
19,2д) | ||||
|
47 |
|
14,4д) | ||||
|
48 |
(H2C=CHCH2)2NH |
19,3 | ||||
|
49 |
(HCºCCH2)2NH |
11,7 | ||||
|
50 |
NCCH2NHCH3 |
2,7з) | ||||
|
51 |
CF3CH2NHCH3 |
6,2з) | ||||
|
52 |
|
12,9 | ||||
|
53 |
|
15,3ж) | ||||
|
54 |
|
4,0ж) | ||||
|
55 |
NHMe-C=O H |
1,7 | ||||
|
56 |
(CH3)3N |
20,0 | ||||
|
57 |
(CH3)2NC2H5 |
22,4 | ||||
|
58 |
(C2H5)2NCH3 |
24,6 | ||||
|
59 |
(C2H5)3N |
26,7 | ||||
|
60 |
(C3H7)3N |
28,7 | ||||
|
61 |
|
17,1и) | ||||
|
62 |
|
8,1и) | ||||
|
63 |
|
24,3 | ||||
|
64 |
|
25,7 | ||||
|
65 |
|
27,1 | ||||
|
66 |
|
26,1к) | ||||
|
67 |
(CH3)2N-NH2 |
15,2 | ||||
|
68 |
((CH3)2NCH2)2 |
30,3 | ||||
|
69 |
|
23,5 | ||||
| ||||||
|
70 |
(H2C=CH-CH2)3N |
24,7 | ||||
|
71 |
(HCºC-CH2)3N |
15,0 | ||||
|
72 |
NCCH2N(CH3)2 |
7,1 | ||||
|
73 |
F3CCH2N(CH3)2 |
20,9 | ||||
|
74 |
|
19,5 | ||||
|
75 |
|
21,0ж) | ||||
|
76 |
|
23,7ж) | ||||
|
77 |
|
19,3 | ||||
|
78 |
|
21,8 | ||||
|
79 |
|
26,0 | ||||
|
80 |
|
16,0 | ||||
|
81 |
CH3CON(CH3)2 |
11,7 | ||||
|
82 |
HCON(CH3)2 |
7,6 | ||||
|
83 |
NF3 |
-56л) |
Смотрите также
Задачи по кинетике цепных, фотохимических и гетерогенных реакций при подготовке школьников к олимпиадам
Физическая
химия – наука, которая изучает общие закономерности физических процессов и
является теоретической основой всей химической науки и технологии химических
производств. Одним из наиб ...
Цель работы
Цель данной работы состоит в разработке схемы
переработки вторичного сырья (в данном случае карбидов тугоплавких металлов
режущих инструментов их осколков, кусковые отходы), при заданных
производит ...
Синтезы органических соединений на основе оксида углерода
Помимо синтезов органических соединений из СО и Н2
– углеводороды, олефины, в том числе изобутилен с высокими показателями
(селективность > 90%), спирты, в том числе изобутанол с выходом ...