Константа химического равновесия в смеси идеальных газов
Рабочие формулы:
Вариант 1. Здесь представлены электронные суммы состояний. Их следует вычислять по отдельности. Электронные уровни должны быть выражены в единой шкале. Этот способ строгий, но менее доступный:
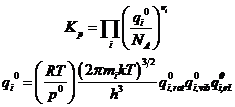
Вариант 2. Здесь представлены кратности вырождения электронных уровней и разность электронных уровней. Этот способ удобен для расчёта диссоциативных равновесий:
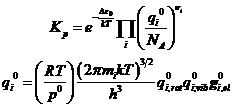
(ВНИМАНИЕ! В учебнике Даниэльса и Олберти в формулах допущены ошибки, связанные с учётом электронных состояний. Здесь ошибки исправлены)
ЗАДАЧИ (с примерами решений) (из Даниэльса – Олберти и из задачника МГУ - Ерёмин и соавторы – см. Литература)
ЗАДАЧА 1.
У молекулы с массой M четыре квантовых состояния распределены между двумя энергетическими уровнями. Спектр уровней определён в виде массива: (0, E, E, E).
Нарисуйте энергетическую диаграмму состояний.
Как называют подобные уровни?
Каковы средние мольные доли частиц, заселяющих эти уровни при температуре T?
Сколько частиц в среднем будет заселять эти уровни в коллективе из N частиц?
Какова поступательная энтропия газа с этими характеристиками в объёме V?
Каково давление этого газа?
При каких температурах:
а) - все частицы будут находиться на основном уровне?
б) - все частицы будут поровну заселять оба уровня?
В) - заселённости всех квантовых состояний равны?
Запишите выражение для средней энергии этого газа и покажите, как она изменяется с увеличением температуры?
ЗАДАЧА 2.
У молекулы с массой M три квантовых состояния относятся к трём энергетическим уровням. Спектр уровней определён в виде массива: (E1, E2, E3).
Нарисуйте энергетическую диаграмму состояний.
Рассчитайте мольные доли частиц, заселяющих эти уровни при температуре T.
Рассчитайте среднюю энергию частицы при температуре T.
Рассчитайте энергию коллектива из N частиц при температуре T.
Можете решать задачу, придав уровням определённые численные значения, например
(E1, E2, E3) = (A, B, C).
ЗАДАЧА 3.
У молекулы с массой M энергетический спектр задан массивом: (0,E1, E2).
Уровни вырождены. Их кратности вырождения равны (g1, g2, g3) =(1, 2, 3), так что коллектив из N частиц распределяется между шестью возможными квантовыми состояниями. Для этого коллектива нарисуйте энергетическую диаграмму состояний, рассчитайте мольные доли частиц, заселяющих эти уровни при температуре T, рассчитайте среднюю энергию одной частицы.
Можете придать уровням определённые значения.
ЗАДАЧА 4.
Запишите выражение поступательной статистической суммы с учётом неразличимости частиц. Рассчитайте при T=300 K поступательную энтропию:
а) газообразного аргона.
б) газообразного водорода для его трёх изотопов: протия 1H, дейтерия D (2H), трития T (3H)].
в) газообразного молекулярного азота (изотопы 14N и 15N).
ПРИМЕЧАНИЕ: Для изотопозамещённых молекул используйте приближённое (но почти точное) правило, согласно которому силовая константа колебания не изменяется при замене атома его изотопом.
ЗАДАЧА 5.
Запишите выражение поступательной вращательной статистической суммы при T=300 K с учётом числа симметрии молекул.
Рассчитайте вращательную энтропию:
а) молекулярного азота (изотоп 14N) при T=300 K.
б) молекулярного кислорода (изотоп 16O) при T=300 K.
Недостающие данные можно взять из справочника
ЗАДАЧА 6.
Запишите выражение колебательной статистической суммы при T=300 K с учётом числа симметрии молекул. Рассчитайте колебательную энтропию:
а) молекулярного водорода для его трёх изотопов (1H; 2D; 3T) при T=300 K.
б) молекулярного азота (изотоп 14N).
Недостающие данные можно взять из справочника.
ЗАДАЧА 7.
Рассчитать при 298 К константу равновесия для реакции изотопного обмена: D+H2=H+DH.
Считать, что равновесные расстояния и энергии диссоциации молекул H2 и DH одинаковы.
(Ответ в учебнике Д-О: K=7.17 ).
РЕШЕНИЕ
Таблица 1. Структурные параметры молекул и изотопов атома водорода.
|
Qяд= = gяд |
Qэл= = gэл |
M, у. е. |
, у. е. |
|
|
D, кДж/моль | |
|
D |
3 |
2 |
2 |
|
- | ||
|
H2 |
1(+3) |
1 |
2 |
½ |
2 |
4395.24 |
431.9802 |
|
H |
2 |
2 |
|
|
- | ||
|
DH |
3´2 |
1 |
3 |
2/3 |
- |
4395.24 |
431.9802 |
Смотрите также
Получение алканов, алкенов, алкинов. Важнейшие представители. Применение в промышленности
Предельными углеводородами (алканами) называются соединения,
состоящие из атомов углерода и водорода, соединенных между собой только
Q-связями, и не содержащие циклов. В алканах атомы углеро ...
Заключение.
В настоящее время человечество
переживает углеводородную эру. Нефтяная отрасль является главной для мировой
экономики. В нашей стране эта зависимость особенно высока. К сожалению российская
нефтяна ...
Расчет проектной себестоимости продукции.
В
курсовом проекте в зависимости от характера продукции, выпускаемой
проектируемым объектом, рассчитывается ее полная или производственная
себестоимость, или внутрицеховые затраты по данному переде ...
