Подгруппа селена.
Теплоты атомизации селена и теллура при 25 °С равны соответственно 226 и 192 кДж/моль.
Друг с другом селен и теллур не соединяются (но смешанные кристаллы образуют). Селен способен соединяться с серой, давая циклические смешанные молекулы SnSе8-n и образованные ими кристаллы, примерами которых могут служить красные Sе4S4, (т. пл. 113 °C) и светло-оранжевые Sе2S6 (т. пл. 122 °С). Для теллура было получено соединение с серой состава ТеS7.
Теллур уже при обычных условиях очень медленно взаимодействует с водой по схеме:
Те + 2 Н2О = ТеО2 + 2 Н2
При нагревании подобным же образом реагирует с водой и аморфный селен, тогда как кристаллический не взаимодействует с ней даже при 150 °С. Оба элемента растворяются в растворах Nа2Sn с образованием ионов SеS22- или ТеS32-. Mелкораздробленные Sе и Те растворяются в холодной концентрированной серной кислоте. Установлено, что растворение идет с образованием желтых ионов Sе42+, зеленых Sе82+ или красных Те42+. При разбавлении раствора водой происходит обратное выделение Sе или Те. Из раствора теллура в жидком серном ангидриде избыток SO3, может быть удалён нагреванием. Дальнейшее нагревание полученного таким путем ТеSO4, сопровождается отщеплением SO2 и образованием черного твердого вещества, по составу отвечающего формуле ТеО (но представляющего собой, по-видимому, смесь ТеО2 + Те). Полоний ведет себя аналогично теллуру, давая красный РоSO3 и черный РоО.
Повышенное содержание селена в почвах может обусловить частичное замещение им серы при построении белковых молекул растительных организмов. Результатом являются заболевания как самих растений, так и питающихся ими животных: у скота выпадает шерсть, размягчаются копыта и т. д. Отмечалось избирательное накопление селена мухоморами.
При приеме внутрь соединения селена действуют подобно мышьяку. После отравлений ими появляется очень неприятный запах от всего тела и выдыхаемого воздуха. Газообразные производные селена уже в ничтожных концентрациях вызывают головную боль, раздражение верхних дыхательных путей, продолжительную потерю обоняния и затяжной насморк. При попадании его соединений на кожу образуются сыпи и болезненные воспаления. Вместе с тем ничтожные дозы селенитов (порядка 3 мкг на 100 г пищи), по-видимому, предотвращают заболевания некротического характера. Отмечалось также прямая связь между остротой зрения животных и содержанием селена в сетчатке их глаз.
|
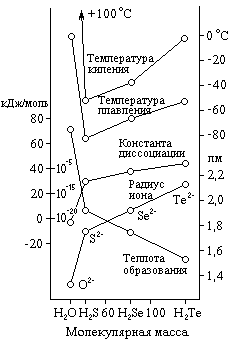
Рис. 3. Свойства водородных соединений элементов VI группы. |
Соединения теллура значительно менее ядовиты. В организме они быстро восстанавливаются до элементарного Те, который затем медленно выделяется в виде постепенно образующихся органических производных, обладающих сильнейшим чесночным запасом. Последний появляется после поступления в организм даже ничтожных количеств Те (десятимиллионных долей грамма). Известен случай, когда работавшим с теллуристыми соединениями химикам пришлось на несколько недель выселиться из города, так как исходивший от них запах был невыносим для окружающих. При лечении селеновых и теллуровых отравлений рекомендуется принимать в повышенных дозах витамин С (аскорбиновую кислоту).
Недавно проведенными исследованиями установлено постоянное наличие следов полония в табачном дыме. Оказалось, что с дымом от пачки сигарет человек поглощает такую дозу облучения a-частицами, которая в 4 раза превышает признаваемую безопасной по международному соглашению. Анализ мочи курильщиков показал, что она содержит полония в 6 раз больше, чем у некурящих. Это значит, что полоний циркулирует по организму и может накапливаться (как и продукт его распада — свинец) не только в легких, но и в любом другом органе. Предполагается, что статистически установленная значительно большая частота заболеваний раком курильщиков по сравнению с некурящими обусловлена главным образом именно радиоактивностью полония.
С химической стороны селен и теллур в общем похожи на серу. Из неметаллов они наиболее энергично взаимодействуют с фтором и хлором, а с кислородом соединяются лишь после предварительного нагревания. С газообразным водородом частично реагирует при повышенных температурах только селен, тогда как теллур с ним непосредственно не соединяется. Со многими металлами Se и Te дают при нагревании аналогичные сульфидам селениды и теллуриды (например, K2Se, K2Te).
Действием на них разбавленных кислот могут быть получены селеноводород (H2Se) и теллуроводород (H2Te). Оба они при обычных условиях представляют собой бесцветные газы с неприятными запахами. Растворимость их в воде примерно такая же, как у сероводорода, причем растворы показывают ясно выраженную кислую реакцию. Некоторые свойства рассматриваемых соединений сопоставлены в приводимой ниже таблице и на рис. 3 с аналогичными свойствами H2O и H2S. Для приблизительной ориентировки в размерах соответствующих молекул приведены также радиусы ионов Э2–.
|
Соединения |
Теплота образования, кДж/моль |
Температура плавления, °С |
Температура кипения, °С |
Константа диссоциации K1 |
Радиус иона Э2–, пм |
|
H2O |
68,5 |
0 |
100 |
2·10-16 |
1,32 |
|
H2S |
5 |
–86 |
–60 |
1·10-7 |
1,74 |
|
H2Se |
–8 |
–66 |
–41 |
1·10-4 |
1,91 |
|
H2Te |
–24 |
–51 |
–2 |
2·10-3 |
2,11 |
Смотрите также
Присадки к современным дизельным топливам.
Зимние
дизельные топлива с депрессорными присадками. С 1981 г. вырабатывают зимнее дизельное топливо марки
ДЗп по ТУ 38.101889— 81. Получают его на базе летнего дизельного топлива с tп =
-5 °С. Доб ...