Цепные разветвлённые реакции
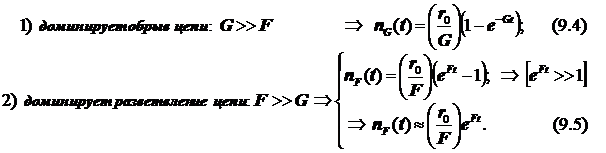
В результате конкуренции разветвления и обрыва возникает специфический механизм цепной разветвлённой реакции, зависящий от многих факторов. В книге Лейдлера (стр.194) рассматриваются взрывные пределы этой реакции. Цитируем: “Реакция водорода с кислородом протекает со скоростями, удобными для измерения между 450 и 600о С; выше этого интервала все смеси взрываются. Если стехиометрическую смесь (H2;O2) держать при (T; p)=(550 оС; 2 тор), то протекает гомогенная реакция. С постепенным повышением давления скорость реакции увеличивается. При некотором критическом давлении, величиною в несколько миллиметров (его точное значение зависит от размеров и формы реакционного сосуда), смесь взрывается. Если смесь выдерживать при p =200 тор, то вновь протекает спокойная стационарная реакция, но, если давление понизить, то при p =100 тор смесь взорвётся. Таким образом, при этой температуре имеется некоторый интервал давлений, внутри которого наблюдается взрыв, а выше и ниже его реакция протекает со стационарной скоростью. Выше 600 оС смесь взрывается при всех давлениях, а ниже 400 оС не взрывается совсем. Два взрывных предела называют первым и вторым или верхним и нижним.
Существует также и третий предел при ещё более высоких давлениях. Иногда этот третий предел является просто термическим пределом; и в этих случаях скорости реакций становятся настолько высокими, что условие изотермичности не сохраняется. Такие взрывы, которые происходят за счёт повышения температуры реакционной системы, называют термическими (тепловыми) . Существуют доводы и в пользу того, что взрыв при третьем пределе в системе (H2;O2) не является термическим, а происходит за счёт внезапного повышения концентрации активных центров-свободных радикалов .”.
Представим исходные состояния реакционной смеси в виде диаграммы в координатах температура – давление (T-p). Координатная плоскость оказывается разделённой на две области Z -образной кривой (-aebdc-) (рис.).
|
t
| |||||||||||||||||||
|
t
| ||||||||||||||||
Смотрите также
Основание СНПЗ, люди завода 40е - 50е годы
Характер проекта:
междисциплинарный
Раздел науки: химия,
история, экономика, экология.
Тип проекта:
информационный, неисследовательский, поисковый, групповой, долгосрочный.
...
Элементарная биохимия
БИОХИМИЯ (биологическая химия) – биологическая наука, изучающая
химическую природу веществ, входящих в состав живых организмов, их превращения
и связь этих превращений с деятельностью органо ...