Кинетический анализ реакций синтеза.
Предметом химической кинетики являются скорости реакций со всеми влияющими на них факторами и интерпретация скорости реакций на основе их механизма. В этом смысле кинетика отличается от термодинамики, в которой рассматриваются начальное и конечное состояния системы вне зависимости от времени протекания этого превращения. Термодинамика обычно рассматривает системы в состоянии равновесия, т. е. в состоянии, в котором скорости прямой и обратной реакций в обратимом процессе равны, что связывает эти две области химии. Однако обратное не верно: скорость реакции нельзя определить только на основе термодинамических данных. Химическую кинетику можно считать более фундаментальной областью науки, но, к сожалению, часто сложность исследуемых процессов делает применение теории химической кинетики довольно трудным.
Рассмотрим равновесие водород -йод в газовой фазе при высокой температуре:
Н2 + I2 = 2НI
Эта реакция протекает при бимолекулярных столкновениях между молекулами йода и водорода, так что стехиометрическое уравнение в этом случае соответствует истинному механизму взаимодействия. Доказательством правильности такого механизма является то, что скорость образования йодистого водорода, как было показано, пропорциональна как концентрации водорода, так и концентрации йода, т. е.
![]()
Это, однако, исключительный случай, так как обычно стехиометрическое уравнение не описывает механизма реакции, как, например, для значительно более сложной реакции водорода с бромом, скорость которой, как было показано, определяется уравнением:
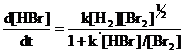
Это можно объяснить следующим механизмом:
![]()
Br + Н2 → НВr + Н (медленная)
Н + Вr2 → НВr + Вr (быстрая)
Н + НВr → Н2 + Вr (быстрая)
Следует отметить, что, зная механизм реакции, не всегда можно дать достаточно определенную интерпретацию экспериментально найденным выражениям для скорости. Иногда с экспериментальными данными согласуются несколько возможных механизмов или вновь полученные данные опровергают ранее принятый механизм.
Очевидно, математическую обработку выражений скоростей реакций через концентрации в определенных степенях
Уравнение:1
![]()
проводить легче, чем для выражений более сложного типа. Только для выражений скорости типа уравнения (1) приемлемо определение порядка реакции n, причем
Уравнение:2
n = n1+n2+n3+……
Из двух рассмотренных выше примеров реакция водорода с йодом -это реакция второго порядка, причем как по водороду, так и по йоду порядок ее равен единице. Понятие порядка реакции неприменимо к взаимодействию водорода с бромом, так как выражение для скорости этого процесса записано не в соответствующей форме.
Если условия проведения реакции таковы, что одна или более концентраций остаются практически постоянными в течение опыта, то эти концентрации можно включить в константу скорости k. В этом случае реакция будет иметь псевдо –n порядок, где n -сумма показателей степеней концентраций, которые в течение эксперимента изменяются. Обычно эти показатели степени -простые положительные числа, но в зависимости от сложности реакции они могут быть дробными или даже отрицательными.
Порядок реакции, определяемый уравнением (2), часто путают с молекулярностью реакции, которая определяется числом молекул, участвующих в элементарном процессе столкновения. Таким образом, молекулярность - это теоретическое понятие, проистекающее из принятого механизма реакции, тогда как порядок - величина эмпирическая; эти две величины могут различаться. Однако бимолекулярные реакции обычно имеют второй порядок, а тримолекулярные реакции -третий порядок, но обратное утверждение не всегда верно. Реакция, которая иллюстрирует только что сказанное, -это окисление ионов Fe2+ перекисью водорода. Стехиометрическое уравнение ее выглядит так:
Смотрите также
Хлор
ХЛОР (лат. Chlorum) , Cl - химический элемент VII группы периодич еской системы Менд е леева,
ат омный номер 17, а томная
м асса 35,453; относится к семейству галогенов. При
нормальных усло ...
Каучук, строение, свойства, виды и применение в профессии коммерсанта
Я выбрала тему “Каучук”, так как она тесно
связана с моей профессией “Коммерсант”. Много непродовольственных товаров
изготовлено на основе синтетического каучука: Обувные товары, игрушки, сп ...
