Квантовые числа. Атомные орбитали.
ms= +1/2; –1/2.
Оно получено из опытов Штерна и Герлаха.
Рассмотренные квантовые числа определяют энергию электрона, объем и форму пространства, в котором вероятно его пребывание в околоядерном объеме, т.е. размер, форму и ориентацию орбитали в пространстве.
Так как волновая функция y является решением уравнения Шредингера при всевозможных значениях квантовых чисел, то можно сказать, что волновая функция является в свою очередь функцией рассмотренных квантовых параметров n, l и ml, где:
n= 1, 2, 3, 4,…,
l= 0, 1, 2, 3,…,n–1
ml=–l,…, –1, 0, +1,…, +l
Атомные орбитали. Так как вероятность нахождения электрона в пространстве далеком от ядра очень мала, когда говорят об орбиталях, то имеют в виду такую область вокруг ядра атома внутри которой сосредоточено 90–95% электронного заряда. С точки зрения квантовой механики атомные орбитали являются геометрическим изображением волновой функции y (n, l, ml).

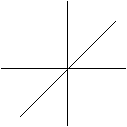 Z Электронное облако. Если бы в каждый момент времени
Z Электронное облако. Если бы в каждый момент времени
![]()
![]() y определяли положение электрона в трехмерном пространстве и
y определяли положение электрона в трехмерном пространстве и
![]()
![]()
![]() ставили в том месте точку, то через множество таких определений
ставили в том месте точку, то через множество таких определений
![]() X получили бы картину в виде пространственного облака изображен-
X получили бы картину в виде пространственного облака изображен-
![]() ного точками с размытыми краями /рис.2.3.)
ного точками с размытыми краями /рис.2.3.)
рис.2.3.
 Такое зарядовое облако называют электронным облаком. Его плотность, пропорциональная y2, является непосредственной мерой вероятности нахождения электрона. Граничная поверхность облака, внутри которой содержится 90–95% электронного заряда, дает форму орбитали.
Такое зарядовое облако называют электронным облаком. Его плотность, пропорциональная y2, является непосредственной мерой вероятности нахождения электрона. Граничная поверхность облака, внутри которой содержится 90–95% электронного заряда, дает форму орбитали.
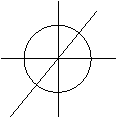 Z s-орбиталь. Она существует при l=0. Значение ml тоже равно
Z s-орбиталь. Она существует при l=0. Значение ml тоже равно
Y нулю. Имеем только одно значение ml =0. Следовательно,
s-орбиталь имеет максимальную симметричность. У нее
X сферическая форма (рис.2.4.). В этом случае вероятность на–
хождения электрона в околоядерном пространстве определя–
рис.2.4. ется только радиусом-вектором и не зависит от угла координат.
y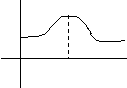 Радиальное распределение электронной плотности для 1s
Радиальное распределение электронной плотности для 1s
электрона соответствует кривой с максимумом (рис.2.5.).
Максимум распространения вероятности находится на
0 r1 r,A0 расстоянии от ядра r1, которые соответствует радиусу
рис.2.5. первой боровской орбиты.
р-орбиталь. Существует при l=1. ml = –1, 0, +1.
![]() Z р-орбиталь появляется на втором и всех последующих
Z р-орбиталь появляется на втором и всех последующих
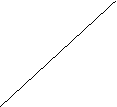
 Рz уровнях. Так как ml имеет три значения, то на р-подуров-
Рz уровнях. Так как ml имеет три значения, то на р-подуров-
Y не каждого уровне может быть три р-орбитали. р-орбиталь
 имеет гонтелеобразную форму. Все три р-орбитали распо-
имеет гонтелеобразную форму. Все три р-орбитали распо-
X лагаются в пространстве по направлению координатных
Px осей. Их называют соответственно рх, рy, рz-орбитали
Py (рис.2.6.).
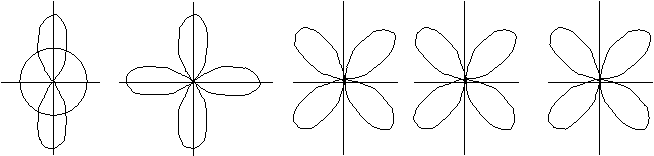 Рис.2.6. Z Y Y Z Z
Рис.2.6. Z Y Y Z Z
X X X X Y
dz2 dx2 y2 dxy dxz dyz
рис.2.7.
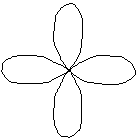
d-орбиталь. Появляется при l=2 на третьем квантовом уровне. На d-подуровне может быть уже пять различных состояний электронов, поэтому на d-подуровне каждого квантового уровня содержится пять d-орбиталей. В этом случае ml принимает пять значений: ml = –2, –1, 0, +1, +2, d-орбитали имеют более сложную форму, чем р-орбитали, они либо в виде четырех лепестков либо в виде гантели с ободком (рис.2.7.).
f-орбиталь. Появляется при значении l=3. f-орбитали могут быть только на четвертом и более отдаленных уровнях. Так как при l=3 ml имеет 7 значений /–3, –2, –1, 0, +1, +2, +3/, то на f-подуровне может быть семь орбиталей. Форма f-орбиталей еще более сложная, чем у d-орбиталей. f-орбитали изображают в виде сложных шестилепестковых фигур.
Смотрите также
Характеристика исходного сырья
Добываемая из скважин эмульсия
представляет собой многофазную систему, состоящую из нефти, пластовой воды и
попутных нефтяных газов. Нефть представляет собой химически сложную компонентную
смесь, ...
Витамины и их значение для организма
Трудно представить, что
такое широко известное слово как «витамин» вошло в наш лексикон только в начале
XX века. Теперь известно, что в основе жизненно важных процессов обмена веществ
в орг ...
Список сокращений
БР
– блок подготовки и закачки реагента.
БРХ
– блок реагентного хозяйства.
ДНС
– ...
