Восстановление и восстановительная циклизация N-(3-оксоалкил) карбоматов при взаимодействии с боргидридом натрия
Восстановление и восстановительная циклизация N-(3-оксоалкил)карбоматов при взаимодействии с боргидридом натрия.
А.С. Фисюк, Е.А. Рыжова, Б.В. Унковский, Омский государственный университет, кафедра органической химии
Известно, что взаимодействие N-(3-oкcoaлкил)карбаматов с комплексными гидридами металлов приводит к N-(3-гидроксиалкил)карбаматам [1, 2] либо продуктам их циклизации -тетрагидро-1,3-оксазин-2-онам [3]. С целью выявления стереонаправленности реакции и факторов, влияющих на глубину ее протекания, нами было изучено взаимодействие соединений Iа-г с боргидридом натрия. Мы установили, что продукты восстановления соединений Iв,д - N-(З-гидроксиалкил)карбаматы Пв,д, выделить не удается, так как в условиях реакции они нестабильны и превращаются в тетрагидро-1,3-оксазин-2-оны IIIв,д. Соединение Iв удалось получить только в нейтральной среде, которую мы поддерживали добавлением в реакционную смесь фосфатного буфера (схема 1).
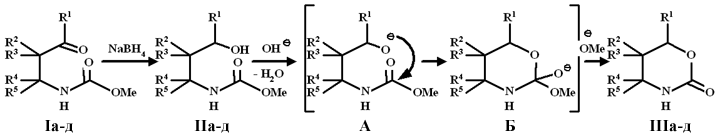
a. R1 = R2 = Me, R3 = R4 = R5 = H ;
б. R1 = R2 = R4 = Me, R3 = R5 = H ;
в. R1 = R4 = R5 = Me, R2 = R3 = H ;
г. R1 = Me, R2 = R5 = H, R3 + R4 = (СH2)4;
д. R3 + R4 = (СH2)4 ; R3, R4 + R5 = (СH2)5 ;
Схема 1.
Метил-N-(3-гидрокси-2-метилбутил)карбамат Iа, имеющий меньшее число заместителей в ал-кильном фрагменте, менее склонен к циклизации по сравнению с IIв,д, что позволило его получить из Iа в отсутствие буферной смеси. Только увеличение рН реакционной среды приводит к превращению На в 1,3-оксазин Ilia. Осуществить циклизацию незамещенного метил-N-(3-гидроксипропил-1)карбамата IIе (R1=R2=R3=R4=R5H) в тетрагидро-1,3-окса-зин-2-он в аналогичных условиях не удается. Аномальное поведение незамещенных циклических карбаматов (их нестабильность при перегонке, склонность к размыканию цикла и полимеризации) отмечалось в работах [4, 5, 6]. В то же время замещенные тетрагидро-1,3-оксазин-2-оны менее склонны к полимеризации [4]. Для объяснения эффекта ускоренной циклизации по-лизамещенных бифункциональных соединений ранее была предложена термодинамическая концепция [7], основанная на. сравнении энтальпии и энтропии для линейных и циклических структур. В ряду замещенных гексанов и циклогексанов показано, что при наличии в цикле алкиль-ных заместителей имеется меньше скошенных несвязанных взаимодействий, чем у соединений с открытыми цепями. Это означает, что энталь-пийные факторы в большей степени благоприятствуют циклизации метилзамещенной цепи по сравнению с незамещенной. Разветвления ограничивают внутреннее вращение, понижают энтропию соединений с открытой цепью, но не могут существенно изменить энтропию циклических соединений, имеющих меньшую свободу внутреннего вращения.
Механизм образования тетрагидро-1,3-окса-зин-2-онов III, вероятно, включает в себя катализируемую основанием циклизацию N-(3-гидроксиалкил)карбаматов в 2-гем-замещенный тетраэдрический интермедиат Б, стабилизирующийся элиминированием метокси- или меркапто-аниона. Повышение рН среды увеличивает скорость реакции за счет увеличения концентрации аниона А.
Взаимодействие карбамата Iг с NaBH4 приводит к смеси (4а,8а-транс,4а,4-транс)- и (4a,8a-транс,4а,4-цис)-4-метилоктагидро-2Н-3,1-бензоксазин-2-онов IIIг, с преобладанием последнего (1/4), в результате циклизации промежуточно образующихся N-(3-гидроксиалкил)карбаматов с конфигурациями анти,анти-IIг и анти,син-IIг. Взаимодействием соединения син-16 с боргидридом натрия была получена смесь оксази-нов 4,5-цис-5,6-транс-IIIб и 4,5-цис-5,6-цис-IIIб в соотношениях 4:1. Состав продуктов восстановительной циклизации карбаматов Iб,г свидетельствует о протекании нуклеофильной атаки атома углерода карбонильной группы гидрид-анионом преимущественно с менее затрудненной стороны , что соответствует "открытой" модели 1,2-асимметрической индукции (схема 2).
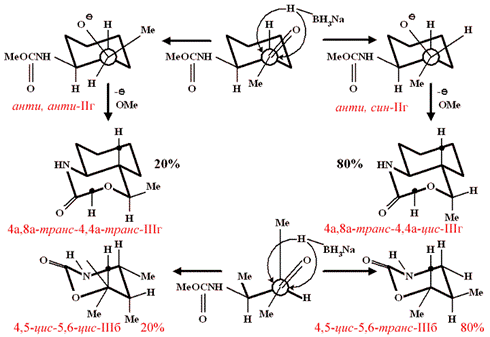
Схема 2.
Таким образом, нами изучено поведение N-(З-оксоалкил)карбаматов в условиях боргидрид-ного восстановления и показано, что в зависимости от рН реакционной среды и строения исходного соединения оно может приводить к образованию Н-(3-гидроксиалкил)карбаматов или тетрагидро-1,3-оксазин-2-онов. Восстановление карбонильной группы протекает диастереоселективно в соответствии с "открытой" моделью 1,2-асимметрической индукции.
Смотрите также
Качественный анализ анионов
Цель аналитической химии - установление качественного и количественного
состава вещества или смеси веществ. В соответствии с этим аналитическая химия делится
на качественный и количественны ...
Основы квантовой механики и ее значение для химии
...
Коксохимическое производство
Основным сырьём для коксохимической промышленности
служат угли. Структура и строение углей могут быть изучены при помощи микроскопа.
Грубая структура угля, обнаруживаемая невооруженным глаз ...
