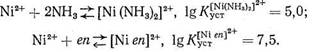Комплексы с полидентатными и макроциклическими лигандами
Основной особенностью биолигандов является их принадлежность к числу полидентатных и (очень часто) макроциклических лигандов.
Как известно, особая устойчивость комплексных соединений, образованных ионами металла с полидентатными лигандами, объясняется образованием одной молекулой (или ионом) лиганда с данным центральным ионом (катионом металла) одного или нескольких хелатных циклов. Согласно правилу Чугаева, наиболее устойчивыми являются пятичленные хелатные циклы (для систем без кратных связей) и шестичленные циклы (для систем с сопряженными двойными связями). Напомним, что энергетическая выгодность замыкания хелатных циклов (хелатный эффект) определяется как энтропийным, так и эн-тальпийным факторами. Рассмотрим в качестве примера комплексообразование Ni2+ с аммиаком и этилендиамином еп:
|
|
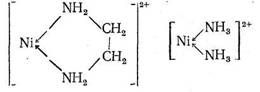
В обоих комплексах ион Ni2+ координирует два атома азота. Большая величина Kуст в случае этилендиаминового комплекса, несомненно, связана с хелатным эффектом: в комплексе [Niеn]2+ имеется пятичленный хелатный цикл, тогда как у комплекса [Ni (NH3)2]2+ — «открытое» строение:
|
|
Координационно насыщенные аммиакаты Ni2+ имеют состав [Ni(NH3)4]2+ или [Ni(NH3)6]2+.
Установлено, что разница в величинах констант устойчивости этих двух комплексов (A lgKуст = 2,5) определяется энтальпийным (∆H= -1,9 ккал/моль) и энтропийным вкладом (∆S = 6,2 кал/град*моль). Разницу в величинах энтальпии образования этих соединений объясняют тем, что в случае [Nien]2+ двум атомам азота, входящим в координационную сферу Ni2+, не нужно преодолевать взаимного отталкиваия (в отличие от комплекса [Ni (NH3)2]2+). Атомы азота этилендиамина уже включены в состав одной молекулы («сближены» друг с другом). Кроме того, при образовании [Niеn]2+ меньше энергии требуется для дегидратации лиганда, чем в случае [Ni (NH3)2]2+: молекулы аммиака меньше по размеру, чем еп, они сильнее гидратируются.
Разница в величинах энтропийных факторов при образовании хелатного и «открытого» комплексов обусловлена увеличением числа частиц при протекании реакции тогда как при синтезе в водном
![]()
растворе диаммиаката никеля (II) в результате комплексообразования число частиц не меняется:
|
|
что связано с бидентатностью еп и монодентатностью NH3.
Как указывает Яцимирский, кроме хелатного эффекта в природных металлокомплексах, образованных биолигандами, часто осуществляется макроциклический эффект. В качестве примера рассматриваются термодинамические характеристики комплексов меди с лигандами L` и L" одинаковой дентатности и сходной природы, но только в L" цепь замкнута в макроцикл:
Смотрите также
Свинцовые аккумуляторы
Кислотные свинцовые
аккумуляторы являются наиболее распространенными
среди вторичных
химических источников тока. Обладая сравнительно высокой
мощностью в сочетании
с надежностью и ...
Технологии для улучшения экологических и эксплуатационных
характеристик дизельных топлив
Экологически
чистое дизельное топливо выпускают
по ТУ 38.1011348—89. Технические условия предусматривают выпуск двух марок
летнего (ДЛЭЧ-В и ДЛЭЧ) и одной марки зимнего (ДЗЭЧ) дизельного топлива с
...
Использование альтернативных источников энергии
Во второй половине ХХ столетия перед
человечеством восстала глобальное проблема – это загрязнение окружающей среды
продуктами сгорания органического топлива. Даже если рассматривать отдельно ...