2. Термодинамические параметры. Термодинамические показатели. Баланс напряжений
. Q не является функцией состояния и не является полным дифференциалом ΔQ.
Понятие работы
Работа процесса
– это энергия, передаваемая одним телом другому при их взаимодействии, не зависящая от температуры этих тел и не связанная с переносом вещества от одного тела к другому.
Обмен энергией между системой и внешней средой обуславливается работой, совершаемой этой системой:
А = PdV.
Работа (А) определяется суммой произведений сил, действующих на систему сил (давления и изменения объема).
Работа не является полным дифференциалом, ΔА
.
Если протекают равновесные процессы, то работа равновесного процесса будет максимальной величиной, по сравнению с неравновесным процессом
ΔAравн > ΔAнеравн.
Если телу сообщают определенное количество теплоты, то это значит, что тело надо нагреть, а охладить систему – произвести действие, обратное нагреванию, т. е. отвести энергию.
Работа и теплота являются количественными характеристиками двух форм обмена энергией между системой и окружающей средой.
Понятие внутренней энергии
Внутренняя энергия системы Uвн
складывается из энергии поступательного и вращательного движения молекул, энергии внутримолекулярного колебательного движений атомов и атомных групп, энергии, заключающейся в ядрах атомов, энергии межмолекулярного взаимодействия.
Uвн является полным дифференциалом, она не зависит от пути процесса, а зависит от начального и конечного состояний системы, она однозначно непрерывна и конечна. Абсолютное значение Uвн определить нельзя, можно определить только ее изменения.
Q и А качественно и количественно характеризуют форму передачи энергии, взаимосвязь между Q, A, Uвн устанавливает первый закон термодинамики.
Термодинамические показатели
К термодинамическим показателям относятся те, которые можно рассчитать, используя законы термодинамики, исходя из условий, что система находится в равновесии. Напряжение разложения: 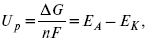
где ΔG – изменение термодинамического потенциала;
п – число электронов, участвующих в химической реакции;
F– число Фарадея. 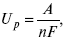
где А – максимальная работа, которую способна совершить система в равновесном состоянии. 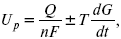
где Q – тепловой эффект реакций;
Up – термодинамическая характеристика электрохимической системы, которая мало зависит от условий электролиза.
Отклонение системы – поляризация. Электрохимическая реакция является гетерогенным процессом, и ее скорость может лимитироваться одной из стадий:
1) подвод реагирующего вещества к границе раздела фаз;
2) разряд и ионизация;
3) отвод продуктов реакции.
Поляризация, определяемая медленной стадией массопереноса – концентрационная. Если медленной стадией является стадия разряда ионизации, то поляризация называется перенапряжением
. Природа и значение поляризации зависят от многих факторов: природа реагирующего вещества, материал электрода, состояние поверхности электрода, плотность тока, состав раствора и режим электролиза. Кинетический параметр
– параметр, определяемый в реальных условиях электрохимической системы: ρ тока, Е АКТИВ, коэффициент диффузии, коэффициент переноса α (на катод), β (на анод) – доля расхода на процесс:
1) сила тока в электрохимическом аппарате J= iKS ед загрузки, A, Z, iK – в зависимости от электролита;
Смотрите также
Улучшение смазочных свойств дизельных топлив
Топлива
в дизельных двигателях являются смазочным материалом для движущихся деталей
топливной аппаратуры, трущихся пар плунжерных топливных насосов. В связи с этим
они должны обладать хорошими прот ...
Поиск структурно-химической информации в Internet
1.а)
Дифракционные методы-рентгеноструктурный анализ и нейронография-как важнейшие
источники структурно-химической информации.
б) Их основы, возможности и ограничения.
в) ...
Приложение 3
Задолженность республик
бывшего СССР
(по состоянию на 01.08.93
г.), млрд.руб.
____________________________________________________________________
Республики н ...
