Притяжение между полимером и поверхностно-активным веществом: влияние природы обоих компонентов
Для описания свойств растворов смесей полимера с ПАВ используются два подхода:
1) взаимодействие рассматривается в рамках сильной кооперативной ассоциации или связывания молекул ПАВ с полимером;
2) взаимодействие представляется моделью мицеллообразования на полимерной цепи или вблизи нее. Эти модели в какой-то мере перекрываются и широко используются в литературе. В то же время модель связывания больше подходит для описания взаимодействия ПАВ и полимеров с гидрофобными группами, а для взаимодействия ПАВ с гидрофильными гомополимерами преимущественно применима модель мицеллообразования.

Рис. 4. Ассоциация гомополимера с ПАВ в различных концентрационных областях. I — При низких концентрациях ПАВ ассоциации не происходит при любых концентрациях полимера. II — При концентрациях выше KKA ассоциация увеличивается вплоть до определенной концентрации ПАВ, которая линейно растет с увеличением концентрации полимера. III — Ассоциация достигает насыщения и концентрация молекулярного ПАВ увеличивается. IV — Область сосуществования ассоциатов ПАВ с полимерными цепями и свободных мицелл ПАВ.
Приведенная диаграмма схематична, но она дает удовлетворительное описание поведения смесей ионных ПАВ и незаряженных гомополимеров в водных растворах
Структура агрегата в смешанных растворах ионных ПАВ и гомополимеров представляется общепринятой моделью «жемчужного ожерелья» (рис. 5): молекулы ПАВ образуют вдоль полимерной цепи мицеллоподобные кластеры. Размер мицелл на полимере совпадает с размерами, характерными для мицелл в водных растворах ПАВ в отсутствие полимера; числа агрегации также близки либо немного ниже, чем в отсутствие полимера в системе.
В присутствии полимера химический потенциал ПАВ понижен по сравнению с водными растворами без добавок полимера (рис. 6).
За связывание ПАВ или мицеллообразование на полимерной цепи отвечают взаимодействия различной природы. Во многих отношениях эти взаимодействия аналогичны взаимодействиям, приводящим к мицеллообразованию в отсутствие полимера. Об этом свидетельствуют данные, полученные при исследовании влияния длины алкильной цепи ПАВ на взаимодействие с полимером, структуры и динамики мицелл и солюбилизации. Изменение свободной энергии системы при ассоциации в основном определяется гидрофобными взаимодействиями алкильных цепей с гидрофобными группами полимера. Но на это взаимодействие оказывает влияние, по крайней мере, один из двух следующих факторов.
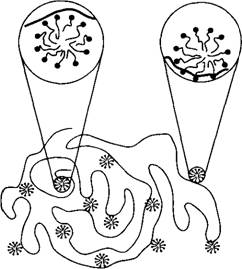
Рис. 5. Модель «жемчужного ожерелья», описывающая ассоциацию ПАВ с полимером
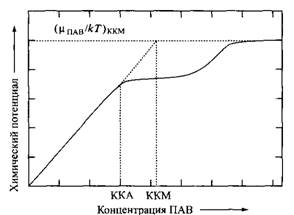
Рис. 6. В присутствии полимера химический потенциал может уменьшаться, что приводит к мицеллообразованию при более низких концентрациях. Приведена зависимость химического потенциала м, деленного на кТ, от логарифма концентрации ПАВ. В присутствии полимера химический потенциал понижен, что индуцирует мицеллообразование на полимере при более низкой концентрации (ККА), чем в отсутствие полимера (ККМ)
В случае полимеров с протяженными гидрофобными участками или гидрофобными группами гидрофобные взаимодействия возникают между соответствующими участками полимера и гидрофобными «хвостами» молекул ПАВ. Такие взаимодействия особенно сильны для блок-сополимеров с гидрофобными и гидрофильными блоками и для привитых сополимеров, в которых гидрофобные группы привиты к гидрофильной основной цепи. Но и гомополимеры также могут иметь неполярные группы разной степени гидрофобное сильные, как в поли (стиролсульфонате), или слабые, как в поли (этиленгликоле). Полярность гидрофобных групп ПЭГ уменьшается с повышением температуры.
Электростатические взаимодействия, очевидно, существуют, если молекулы и полимера, и ПАВ заряжены. Если заряды противоположны по знаку, электростатические взаимодействия приводят к сильной ассоциации компонентов. Однако необходимо учитывать отталкивание между молекулами заряженного полимера, как и между заряженными молекулами поверхностно-активного вещества. Как уже обсуждалось ранее, в случае ионных ПАВ энтропийный проигрыш при самоассоциации ПАВ определяется повышенной концентрацией противо-ионов на поверхности агрегата по сравнению с их концентрацией в растворе. Такое изменение энтропии препятствует самоассоциации молекул и объясняет в том числе, почему KKM ионных ПАВ на порядок больше, чем KKM неионных ПАВ.
Молекулы полимера могут различным образом влиять на изменение энтропии в системе. Если молекулы полимера заряжены и несут такой же заряд, в системе просто будет проявляться умеренный электролитный эффект. Если заряд полимера противоположен по знаку, он действует как многовалентный электролит. Взаимодействие между компонентами усиливается, поскольку в результате ассоциации полимера с мицеллами ПАВ высвобождаются противоионы и полимера, и мицелл. Подобный эффект наблюдается и при взаимодействии двух противоположно заряженных полимеров. В таких случаях происходит уменьшение значений KKM на порядки.
Смотрите также
Природа взаимодействий белков
Белковые вещества составляют громадный класс органических, то есть углеродистых, а именно углеродисто азотистых соединений, неизбежно встречаемых в каждом организме. Роль белков в организме огромна. ...
Алкалоиды маклейи
Цель работы
- Знакомство с
химическим строением и свойствами алкалоидов маклейи мелкоплодной
- Использование
свойств алкалоидов маклейи для их выделения из растительного сырья.
...
Металлы жизни
...
