Химические свойства
1. Образование солей.
Первичные и вторичные нитросоединения растворимы в щелочах с образованием солей. Это объясняется тем, что водородные атомы пр углероде, связанном непосредственно с нитрогруппой, под влиянием последней активируются, и в щелочной среде нитросоединения перегруппировываются в аци-нитро-форму (кислотную
):
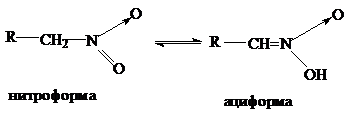
Таким образом, нитроалканы являются таутомерными веществами, существующими в нитро- и аци-нитро-формах.
Если щелочные растворы нитросоединений обработать минеральной кислотой, то происходит медленный обратный сдвиг равновесия:
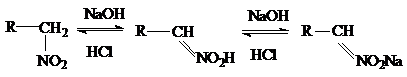
Поэтому нитросоединения относят к псевдокислотам
. Для псевдокислот характерно, что сами они нейтральны, не обладают электропроводностью, но образуют нейтральные соли щелочных металлов. «Нейтрализация» нитросоединений основаниями (образование нейтральных солей) происходит медленно, а истинных кислот - мгновенно.
2. Образование аминов (восстановление) - см. Лекцию №32.
3. Реакции с азотистой кислотой.
Активность водородных атомов у углерода, непосредственно связанного с нитрогруппой, проявляется и в ряде других реакций, например, в реакциях с азотистой кислотой. Первичные и вторичные нитросоединения реагируют с азотистой кислотой, а третичные не реагируют:
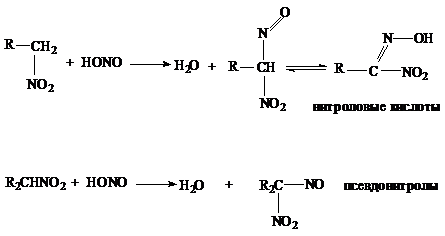
Щелочные соли нитроловых кислот в растворе имеют красный цвет. Псевдонитролы в растворах и расплавах окрашены в синий или зеленовато-синий цвет.
4. Конденсация с альдегидами.
Первичные и вторичные нитросоединения конденсируются с альдегидами, образуя нитроспирты:
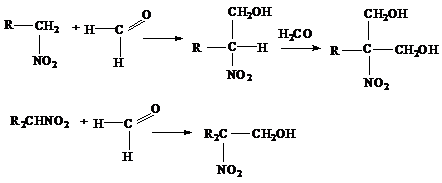
Нитрометан с формальдегидом дает триметилолнитрометан NO2-C(CH2OH)3. При восстановлении последнего получается аминоспирт NH2-C(CH2OH)3, используемый в производстве моющих средств и эмульгаторов. Азотнокислые эфиры нитроспиртов, например, NO2-C(CH2ONO2)3, являются ценными взрывчатыми веществами.
5. Образование альдегидов и кетонов.
Аци-формы первичных и вторичных спиртов нитросоединений в водных растворах при действии минеральных кислот образуют альдегиды или кетоны:

6. Образование карбоновых кислот.
Первичные нитросоединения при нагревании 85%-ной серной кислоты переходят в карбоновые кислоты с отщеплением гидроксиламина. Реакция может служить промышленным способом получения гидроксиламина:

Нитропарафины
используют в технике как растворители, для производства альдегидов, кислот, взрывчатых веществ, в реактивной технике, резиновой промышленности (вулканизаторы), при изготовлении пластмасс и др.
Смотрите также
Полимеры и их конформации
Полимерные молекулы представляют собой обширный класс соединений,
основными отличительными характеристиками которых являются большая
молекулярная масса и высокая конформационная гибкость цеп ...
Каучук, строение, свойства, виды и применение в профессии коммерсанта
Я выбрала тему “Каучук”, так как она тесно
связана с моей профессией “Коммерсант”. Много непродовольственных товаров
изготовлено на основе синтетического каучука: Обувные товары, игрушки, сп ...
Введение
В настоящее время развитие
производств, применяющих смесь азотной и серных кислот в качестве нитрующего
агента, привело к получению огромных количеств отработанных кислотных смесей.
Эти смеси с эк ...
