Адсорбция и адсобционные равновесия
Подставляя величину концентрации в уравнение константы, получим выражения
![]() , св = с,
, св = с,
А = А¥Кс – АКс, ![]() - для жидкостей;
- для жидкостей;
![]() - для газов.
- для газов.
Эти выражения – уравнения изотермы адсорбции Ленгмюра. К и Кр в уравнении характеризуют энергию взаимодействия адсорбента с адсорбатом. Адсорбционное уравнение часто представляют относительно степени заполнения поверхности, т.е. как отношение А/А¥:
![]() ,
,
![]() .
.
Экспериментальные результаты по определению изотермы адсорбции обычно обрабатывают с помощью уравнения, записанного в линейной форме;
![]() , т.е. уравнение типа y = b + ax.
, т.е. уравнение типа y = b + ax.
Такая линейная зависимость позволяет графически определить А¥ и К. Зная А¥, можно определить удельную поверхность адсорбента (поверхность единицы массы адсорбента):
![]() ,
,
где А¥ - предельная адсорбция, выражаемая числом молей адсорбата на единицу массы адсорбента;
NA – число Авогадро;
w0 – площадь, занимаемая одной молекулой адсорбата.
1. Если сà 0, тогда уравнение примет вид:
А=А¥Кс; ![]() ; А = Кгс, q =Кс,
; А = Кгс, q =Кс,
т.е. при сà 0 уравнение Ленгмюра переходит в уравнение Генри.
2. Если сà¥, тогда А = А¥ , А/А¥ = 1. Это случай предельной адсорбции.
3. Пусть адсорбция идет из смеси компонентов, в этом случае уравнение Ленгмюра записывается следующим образом:
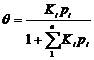 .
.
Все рассмотренные выше уравнения справедливы для мономолекулярной адсорбции на адсорбенте с энергетически эквивалентными адсорбционными центрами. Однако реальные поверхности этим свойством не обладают. Приближенной к реальности является возможность распределения адсорбционных центров по энергии. Приняв линейное распределение, Темкин
использовал формулу уравнения Ленгмюра и получил уравнение для средних степеней заполнения адсорбента.
![]() ,
,
где - константа, характеризующая линейное распределение;
К0 - константа уравнения Ленгмюра, отвечающая максимальной теплоте адсорбции.
Из уравнения следует, что увеличение парциального давления (из-за увеличения концентрации) одного компонента подавляет адсорбцию другого и тем сильнее, чем больше его адсорбционная константа равновесия. Уравнение часто называют логарифмической изотермой адсорбции. Если принять экспоненциальное распределение центров по поверхности, то в области средних заполнений получается ранее найденное эмпирическим путем уравнение Фрейндлиха:
![]() .
.
Прологарифмировав, получим ![]() ,
,
где K, n – постоянные.
Использование уравнения Фрейндлиха в логарифмической форме позволяет определить константу уравнения.
Уравнение Ленгмюра можно использовать только при адсорбции в мономолекулярном слое. Это условие выполняется при хемосорбции, физической адсорбции газов при меньшем давлении и температуре выше критической.
Смотрите также
Бетулин и его производные
В последние годы, когда береза вовлекается все
больше в химическую переработку, ее экстрактивные вещества исследуют в более
широком аспекте. Одним из основных продуктов её переработки являет ...
Составление квартальной отчетности
Представляется в течение года ежеквартально, состоит из бухгалтерского баланса (форма № 1) и отчета о прибылях и убытках (форма № 2). Хотя по желанию организация может представлять и иные отчетные фор ...
