Лекции по химии
Тепловой эффект х.р. зависит только от вида и состояния исходных в-в и кон продуктов. При термохим рассчетах использ термохим у-ия. Т.х. у-ия обязательно должны содержать молярные кол-ва в-в, в правой части должен быть приведен тепловой эффект, должны быть указаны агрегатные состояния в-в, с т.х. у-иями можно производить все алгебраические действия.
З-н Гесса применим как к хим реакциям так и к физ-хим превращениям (процессам плавления, кристаллизации, испарения, сублимации, конденсации, растворения и т.д.)
При записи з-на Гесса используется два вида тепл эффектов:
1) Энтальпия образования в-в – ΔfH˚ - (тепл эффект реакции образования одного моля данного соединения из простых в-в, взятых в устойчивых стандартных состояниях)
ΔrH˚=ΣконΔfH˚*ni- ΣисхΔfH˚*ni
ΔrH˚ - тепл эффект реакции
ni – стехиометрический коэф
2) Энтальпия сгорания - ΔHсгор - (тепл эффект реакции окисления одного моля данного соединения с кислородом с образованием высших оксидов соответствующих элементов)
ΔrH˚=ΣисхΔHсгор*ni- ΣконΔHсгор*ni
Рассмотрим зависимость теплового эффекта реакции от температуры
Пусть реакция А→В происходит при p=constТепл эффект реакции по з-ну Гесса: ΔrH=HB-HA
Продифференцируем данное у-ие по тем-ре
(dΔrH/dT)p= (dHB/dT)p-(dHA/dT)p
ΔH=Qp
(dΔrH/dT)p=Cp,B-Cp,A – диффер ур-е Кирхгоффа.
Изменение тепл эффекта процесса с температурой = изменению теплоемкости системы, происходящее в результате процесса.
В небольшом интервале температур теплоемкость системы можно считать не зависящей от тем-ры, тогда при p=const, интегрируя дифференциальную формулу (от Т1 до Т2):
ΔHT2=ΔHT1+ΔCP(T2-T1) - интегральное ур-е Кирхгоффа
Т1=298˚К
ΔHT2=ΔH298+ΔCP(T2-298)
По следствию из закона Гесса, изменение теплоемкости находится по следующему соотношению
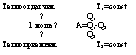 ΔCP=ΣконCP*ni- ΣисхCP*ni
ΔCP=ΣконCP*ni- ΣисхCP*ni
4) (2) нач т/д устанавливает направление и условие протекания естественных процессов, для рассчетов наиболее удобной явл формулировка (2) нач т/д, связанная с ростом энтропии.
Вывод (2) нач т/д сделано на основе анализа работы идеальной тепловой машины
η=A/Q1=(Q1-Q2)/Q1=(T1-T2)/T1
Q1/T1-Q2/T2=<0
δQ1/T1-δQ2/T2=<0
dS=δQ/T - приведенная теплота, отражает измен некот фун-ии состояния
(2) нач т/д:
существует некоторое экстенсивное св-во системы S, называемое энтропией, к-ое связано с поглощаемой теплотой и тем-рой системы следующим образом
а) обр dS=δQ/T
б) необр dS>δQ/T
Все самопроизвольные процессы протекают с увеличением энтропии.
Изменение энтропии (ΔS) не зависит от пути перехода из нач состояния в кон, следовательно не зависит от того какой процесс обратимый или необратимый.
При расчетах реальных систем необр процессы можно представл как совокупность множества обратимых.
ΔS=1∫2(δQ/T)обр
Изотермические процессы Т=const
К ним относится фазовое превращение (испарение, конд и т.д.)
Смотрите также
Проект реконструкции цеха первичной переработки нефти и получения битума на ОАО «Сургутнефтегаз»
...
Присадки к современным дизельным топливам.
Зимние
дизельные топлива с депрессорными присадками. С 1981 г. вырабатывают зимнее дизельное топливо марки
ДЗп по ТУ 38.101889— 81. Получают его на базе летнего дизельного топлива с tп =
-5 °С. Доб ...
Расчет проектной себестоимости продукции.
В
курсовом проекте в зависимости от характера продукции, выпускаемой
проектируемым объектом, рассчитывается ее полная или производственная
себестоимость, или внутрицеховые затраты по данному переде ...
