Общие свойства лантаноидов
Лантаноиды – это 14 элементов, следующих за лантаном, у которых к электронной конфигурации лантана последовательно добавляются 14 4f-электронов. В табл. 2.1 приведены электронные конфигурации лантаноидов и их наиболее устойчивые степени окисления. Общая электронная конфигурация лантаноидов – 4f2–145d0–16s2.
У церия на 4f-уровне находятся два электрона – один за счет увеличения порядкового номера по сравнению с лантаном на единицу, а другой переходит с 5d-уровня на 4f. До гадолиния происходит последовательное увеличение числа электронов на 4f-уровне, а уровень 5d остается незанятым. У гадолиния дополнительный электрон занимает 5d-уровень, давая электронную конфигурацию 4f75d16s2, а у следующего за гадолинием тербия происходит, аналогично церию, переход 5d-электрона на 4f-уровень (4f96s2). Далее до иттербия наблюдается монотонное увеличение числа электронов до 4f14, а у завершающего ряд лютеция вновь появляется 5d-электрон (4f145d16s2).
Таблица 2.1
|
Электронная конфигурация и степени окисления лантаноидов | |||
|
Элемент |
Электронная конфигурация |
Степень окисления | |
|
Церий |
Ce |
4f26s2 |
+3, +4 |
|
Празеодим |
Pr |
4f36s2 |
+3, +4 |
|
Неодим |
Nd |
4f46s2 |
+3 |
|
Прометий |
Pm |
4f56s2 |
+3 |
|
Самарий |
Sm |
4f66s2 |
+2, +3 |
|
Европий |
Eu |
4f76s2 |
+2, +3 |
|
Гадолиний |
Gd |
4f75d16s2 |
+3 |
|
Тербий |
Tb |
4f96s2 |
+3, +4 |
|
Диспрозий |
Dy |
4f106s2 |
+3, +4 |
|
Гольмий |
Ho |
4f116s2 |
+3 |
|
Эрбий |
Er |
4f126s2 |
+3 |
|
Тулий |
Tm |
4f136s2 |
+2, +3 |
|
Иттербий |
Yb |
4f146s2 |
+2, +3 |
|
Лютеций |
Lu |
4f145d16s2 |
+3 |
Периодический характер заполнения 4f-орбиталей сначала по одному, а потом по два электрона предопределяет внутреннюю периодичность свойств лантаноидов. Периодически изменяются металлические радиусы, степени окисления, температуры плавления и кипения, величины магнитных моментов, окраска и другие свойства (Рис. 2.1).
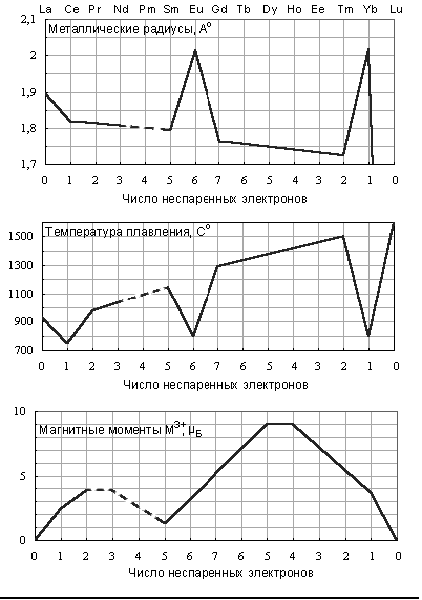
Вторичная периодическая зависимость металлических радиусов, температуры плавления и магнитного момента
Рис. 2.1
Участие 4f-электронов в образовании химической связи обусловлено предварительным возбуждением на уровень 5d. Энергия возбуждения одного электрона невелика, поэтому обычно лантаноиды проявляют степень окисления +3. Однако некоторые из них проявляют так называемые аномальные степени окисления – +2, +4. Эти состояния окисления связывают с образованием наиболее устойчивых электронных конфигураций 4f0, 4f7, 4f14. Так, Ce и Tb приобретают конфигурации f0 и f7, переходя в состояние окисления +4, тогда как Eu и Yb имеют соответственно конфигурации – f7 и f14 в состоянии окисления +2. Однако существование Pr (IV), Sm (II), Dy (IV) и Tm (II) свидетельствует об относительности критерия особой устойчивости электронных конфигураций 4f0, 4f7 и 4f14. Как и для d-элементов, стабильность состояния окисления наряду с этим фактором характеризуется термодинамическими параметрами реального соединения.
Смотрите также
Эволюция и кислород
ИСПОКОН веков людей волновал вопрос, как возникли живой мир и
они сами. Кажущаяся непостижимость происхождения организмов во всей их
сложности и совершенстве неизменно толкала человечество к ...
Биохимия углеводов в организме человека
Важнейшими
химическими соединениями живых организмов являются углеводы. Они широко
распространены в природе, в растительном мире они составляют 70-80% из расчета
на сухое вещество, у животн ...
Синтез 4-метоксифенола
4-Метоксифенол (гидрохинона монометиловый эфир, пара-метоксифенол,
4-Гидроксианизол) – ромбические кристаллы (растворитель перекристаллизации -
вода). Молекулярная масса: 124,14. Температура ...
