Синтез алифатических и ароматических кислот.
Промышленные способы получения ненасыщенных карбоновых кислот.[2].
1.Окисление углеводородов. Существует два способа: окисление низших алканов C4-C8 преимущественно в уксусную кислоту и окисление твердого парафина в синтетические жирные кислоты (СЖК) с прямой цепью углеродных атомов С10-С20, являющихся сырьем для синтеза ПАВ
2. Синтезы на основе оксида углерода (II). Карбоновые кислоты получают на основе оксида углерода по реакции карбонилирования:
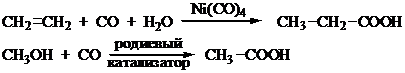
Особый интерес данный метод представляет для синтеза кислот с третичным радикалом (неокислот) из изоолефинов (реакция Коха):
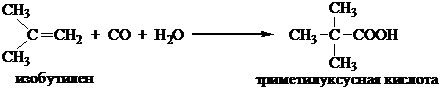
Механизм реакции состоит в предварительном протонировании алкена кислотой с образованием иона карбения, его взаимодействия с СО с получением ацилий – катиона и реакции последнего с водой с образованием карбоновой кислоты:
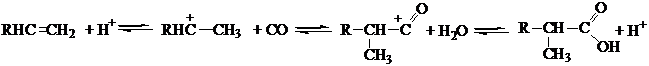
Неокислоты и их соли обладают очень высокой растворимостью и вязкостью, а их сложные эфиры - стабильностью к гидролизу, что обеспечивает им широкое применение в ряде отраслей.
Лабораторные способы получения карбоновых кислот
1.Окисление альдегидов и кетонов.
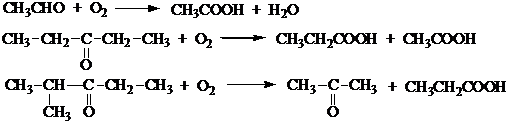
2.Гидролиз нитрилов.
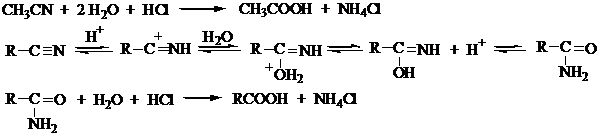 3. Синтез Гриньяра. При взаимодействии магнийорганических соединений с диоксидом углерода образуются соли карбоновых кислот:
3. Синтез Гриньяра. При взаимодействии магнийорганических соединений с диоксидом углерода образуются соли карбоновых кислот:
![]()
Под действием сильной кислоты (обычно НСl) соль превращается в кислоту:
![]()
4. Гидролиз жиров Жиры - сложные эфиры карбоновых кислот и глицерина (триглицериды). Карбоновые кислоты, входящие в состав жиров имеют углеродную цепь от 3 до 18 углеродных атомов. Кипячение жиров или масел с водными растворами щелочей (NaOH, КОН) приводит к получению солей карбоновых кислот и глицерина. Эта операция называется омылением, так как соли карбоновых кислот используют для изготовления мыла.
Методы получения ароматических карбоновых кислот.[3].
Превращение функциональных групп.
1. Окисление ароматических углеводородов.
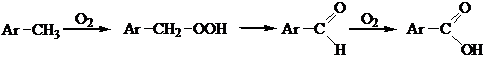
Жидкофазным окислением метилбензолов кислородом воздуха в промышленности получают моно- и дикарбоновые ароматические кислоты.
Окисление можно проводить перманганатом калия в кислой среде:
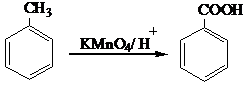
2. Окисление спиртов, альдегидов и кетонов. В качестве окислителя может выступать щелочной раствор перманганата калия, ароматические альдегиды окисляются аммиачным раствором оксида серебра
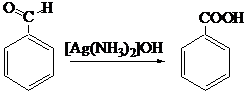
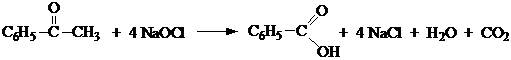
3. Реакция Канниццаро:
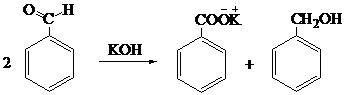
4. Гидролиз галогенпроизводных.
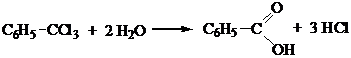
5. Гидролиз нитрилов
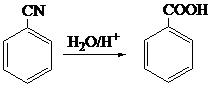
Введение карбоксильной группы в ароматическое ядро
1. Применение фосгена
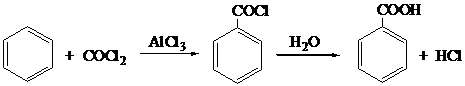
2. Ацилирование эфирами хлоругольной кислоты
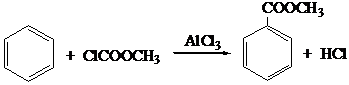
3. Через стадию формилирования
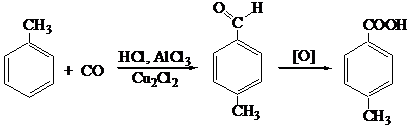
4. Через стадию ацилирования ароматических углеводородов
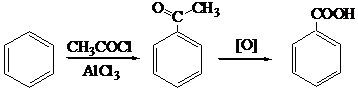
5. Синтез на основе металлоорганических реагентов
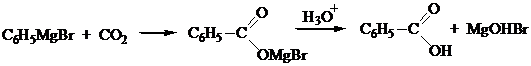
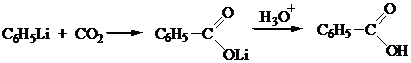
Смотрите также
Этапы определения АК последовательности в пептидах. Синтез белка
Предварительное
освобождение каждого анализируемого пептида от примесей других.
1.
Идентификация NH2- и СООН - концевых остатков.
2.
Расщепление с помощью трипсина неповрежденной цепи ...
Основы теории и основные понятия процесса хроматографического разделения
Процесс
хроматографического разделения очень сложен, тем не менее, его отдельные стадии могут быть смоделированы и представлены в
виде уравнений, достаточно точно и верно отражающих реальный ...
Биохимия углеводов в организме человека
Важнейшими
химическими соединениями живых организмов являются углеводы. Они широко
распространены в природе, в растительном мире они составляют 70-80% из расчета
на сухое вещество, у животн ...
