Сущность кинетики химических процессов.
Δτ–>0
матически определяется производной от концентрации по времени. Она равна тангенсу угла наклона касательной (углаα) к кривой, показывающей форму изменения концентраций от времени (на рис.10.3.) с течением времени. Величина угла наклона
 С
С
k
α
Рис.10.3.
τ
касательной будет убывать, следовательно скорость реакции будет уменьшаться. Она рана тангенсу угла наклона (α) касательной к кривой зависимости концентрации от времени в соответствующий момент времени. (на рис.10.2. точка “k”)
С С
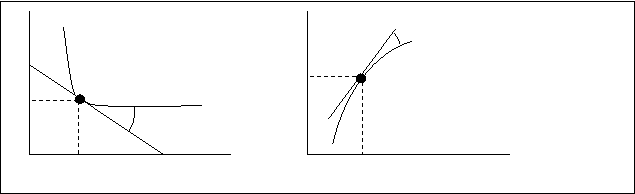 α
α
dc
dc k k
α
dτ τ dτ τ
Рис.10.2.
Vτ =dc/dτ=tgα
Для реакции А+В=Д, VА= -dCА/dτ; VB= -dCB/dτ; VД= +dCД/dτ.
Если для определения скорости реакции брать: количество изменяющегося вещества – количество молей, единицу времени – секунды, а единицу реакционного пространства – литр (для гомогенных систем) и единицу площади межфазового пространства м2 (для гетерогенных систем), то
Vгомоген.=[колич. вещества]/[время] [объем]=моль/с*л;
Vгетероген.=[колич. вещества]/[время] [площадь]=моль/с*м2.
Однак сокорость реакции можно определить по любому компоненту. Выбор вещества обуславливается легкостью, удобством и точностью определения количества вещества в реакционной системе. Например, объем выделеного газа, масса образующегося осадка, изменение кислотности раствора и др. На величину скорости химической реакции влияет множество факторов. Прежде всего это:
¾ природа реагирующих веществ;
¾ их концентраця;
¾ давление (если в реакции участвуют газы);
¾ катализаторы (ингибиторы);
¾ поверхности раздела фаз (для гетерогенных реакций);
¾ степень диффузии.
Смотрите также
Модификация биологически активными системами синтетического полиизопрена
В настоящее
время в резиновой промышленности применяют широкий спектр каучуков, однако
большую часть промышленного потребления составляют натуральный и синтетический
полиизопрены. До сих по ...
Очистка от пестицидов
Пестициды (ядохимикаты) -
химические препараты для защиты сельскохозяйственной продукции, растений, для
уничтожения паразитов у животных, для борьбы с переносчиками опасных
заболеваний и т ...
Кислород
...
