Условия равновесия в многокомпонентных гетерогенных системах.
Пусть р, Т = Const, тогда ![]() . Если в системе имеются фазы (') и (''), то при переходе dni молей i –ого компонента из фазы (') в фазу ('') изменение энергии Гиббса системы dG будет складываться из изменении энергий Гиббса обеих фаз dG ' и dG '':
. Если в системе имеются фазы (') и (''), то при переходе dni молей i –ого компонента из фазы (') в фазу ('') изменение энергии Гиббса системы dG будет складываться из изменении энергий Гиббса обеих фаз dG ' и dG '': ![]() .
.
Если система закрытая, то 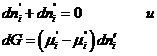 , а если она к тому же и равновесна, то dG = 0 и, следовательно,
, а если она к тому же и равновесна, то dG = 0 и, следовательно, ![]() , т.е. химические потенциалы данного компонента во всех фазах системы, находящейся в равновесии, равны между собой.
, т.е. химические потенциалы данного компонента во всех фазах системы, находящейся в равновесии, равны между собой.
Самопроизвольный неравновесный процесс может идти только в сторону уменьшения энергии Гиббса системы dG < 0 (p, T = const).
Предположим, что ![]() , т.е. фаза (') теряет i –ый компонент, но
, т.е. фаза (') теряет i –ый компонент, но ![]() , значит
, значит ![]() .
.
Если же ![]() , тогда
, тогда ![]() . Таким образом, компонент самопроизвольно переходит из фазы, в которой его химический потенциал больше, в фазу, в которой его химический потенциал меньше.
. Таким образом, компонент самопроизвольно переходит из фазы, в которой его химический потенциал больше, в фазу, в которой его химический потенциал меньше.
Эти условия равновесия и самопроизвольности процессов переноса вещества в многокомпонентных системах являются обобщением таковых для однокомпонентных систем (см. гл. 6). Кроме того, легко заметить, что химический потенциал чистого вещества равен его мольной энергии Гиббса.
Смотрите также
Золото и его переработка
Основные свойства Начинать разговор о золоте лучше всего со свойств
этого металла и только потом переходить к тому, как эти свойства используются
человеком. Золото интересно тем, что в его х ...
Влияние углекислого газа
Деятельность
человека достигла уже такого уровня развития, при котором её влияние на природу
приобретает глобальный характер. Природные системы - атмосфера, суша, океан, -
а также жиз ...
