Квантовые числа
Квантовые числа – это энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится. Квантовые числа необходимы для описания состояния каждого электрона в атоме. Всего 4-ре квантовых числа. Это: главное квантовое число – n, орбитальное квантовое число – l, магнитное квантовое число – ml и спиновое квантовое число – ms.
Главное квантовое число – n.
Главное квантовое число – n – определяет энергетический уровень электрона, удалённость энергетического уровня от ядра и размер электронного облака. Главное квантовое число принимает любые целочисленные значения, начиная с n=1 (n=1,2,3,…) и соответствует номеру периода.
Орбитальное квантовое число – l.
Орбитальное квантовое число – l – определяет геометрическую форму атомной орбитали. Орбитальное квантовое число принимает любые целочисленные значения, начиная с l=0 (l=0,1,2,3,…n-1). Независимо от номера энергетического уровня, каждому значению орбитального квантового числа соответствует орбиталь особой формы. “Набор” таких орбиталей с одинаковыми значениями главного квантового числа называется энергетическим уровнем. Каждому значению орбитального квантового числа соответствует орбиталь особой формы. Значению орбитального квантового числа l=0 соответствует s-орбиталь (1-ин тип). Значению орбитального квантового числа l=1 соответствуют p-орбитали (3-ри типа). Значению орбитального квантового числа l=2 соответствуют d-орбитали (5-ть типов). Значению орбитального квантового числа l=3 соответствуют f-орбитали (7-мь типов).
| Значение орбитального квантового числа – l. |
Типы орбитали. | Количество типов орбитали. |
| l=0 | s-орбиталь | 1 |
| l=1 | p-орбитали | 3 |
| l=2 | d-орбитали | 5 |
| l=3 | f-орбитали | 7 |
s-орбиталь.
p-орбитали.
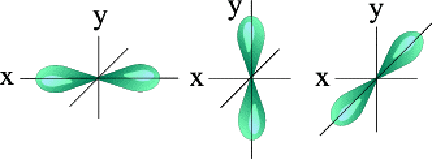
d-орбитали. 
f-орбитали имеют ещё более сложную форму. Каждый тип орбитали – это объём пространства, в котором вероятность нахождения электрона – максимальна.
Магнитное квантовое число – ml.
Магнитное квантовое число – ml – определяет ориентацию орбитали в пространстве относительно внешнего магнитного или электрического поля. Магнитное квантовое число принимает любые целочисленные значения от –l до +l, включая 0. Это означает, что для каждой формы орбитали существует 2l+1 энергетически равноценных ориентаций в пространстве – орбиталей.
Для s-орбитали:
l=0, m=0 – одна равноценная ориентация в пространстве (одна орбиталь).
Для p-орбитали:
l=1, m=-1,0,+1 – три равноценные ориентации в пространстве (три орбитали).
Для d-орбитали:
l=2, m=-2,-1,0,1,2 – пять равноценных ориентаций в пространстве (пять орбиталей).
Для f-орбитали:
l=3, m=-3,-2,-1,0,1,2,3 – семь равноценных ориентаций в пространстве (семь орбиталей).
Спиновое квантовое число – ms.
Спиновое квантовое число – ms – определяет магнитный момент, возникающий при вращении электрона вокруг своей оси. Спиновое квантовое число может принимать лишь два возможных значения +1/2 и –1/2. Они соответствуют двум возможным и противоположным друг другу направлениям собственного магнитного момента электрона – спинам. Для обозначения электронов с различными спинами используются символы: 5 и 6.
Смотрите также
Ароматические ацетаминопроизводные
...
Расчет проектной себестоимости продукции.
В
курсовом проекте в зависимости от характера продукции, выпускаемой
проектируемым объектом, рассчитывается ее полная или производственная
себестоимость, или внутрицеховые затраты по данному переде ...
Пищевые добавки
...
