Валентность в комплексных соединениях.
Недостаточность классического понимания ВАЛЕНТНОСТИ видна также на примере так называемых "нуль-валентных" соединений, где атом металла связан исключительно с нейтральными молекулами; таковы карбонилы металлов типа Ti (CO)7, Cr (CO)6, Fe (CO)5, аммиакаты типа Pt (NH3)4 и т.д. В них вообще отсутствует классическое валентное взаимодействие (у атомов С и N в молекулах CO и NH3 нет неспаренных электронов), а связь осуществляется только за счёт координационных ВАЛЕНТНОСТЕЙ атома металла и молекул лигандовалентность Нейтральные лиганды часто оказываются мостиковыми и образуют по две, например в Co4(CO)12, и даже по три, например в Rh6(CO)16, связи.
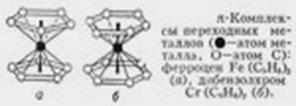 Для теории ВАЛЕНТНОСТИ особый интерес представляют так называемые p-комплексы переходных металлов с ароматическими молекулами или молекулами с сопряжёнными связями в качестве лигандов (этиленом, циклопентадиенилом, бензолом и др.) типа ферроцена Fe (C5H5)2, дибензолхрома Cr(C6H6)2,тетрациклопентадиенила титана Ti (C5H5)4 и др. В отличие от комплексов типа [Сr (NHз)6]3+, [Сr (H2O)6]2+ или Cr (CO)6, где центральный атом осуществляет связь с лигандом через один атом от каждого лиганда (через N - в аммиакатах, через О - в гидратах, и т.д.), в p-комплексах атомы Fe, Cr и Ti взаимодействуют совершенно одинаково со всеми атомами С каждого ароматического кольца. Непригодность классической ВАЛЕНТНОСТИ здесь очевидна: при этом пришлось бы считать все атомы углерода 5-валентными, а атомы Fe, Cr и Ti - соответственно 10-, 12- и 20-валентными. Единственный неспаренный электрон, который имеется у радикала ×C5H5 (так же как и у многих других ароматических радикалов типа тропила ×C7H7 и т.д.), в равной степени принадлежит всем углеродным атомам кольца. Для этого класса соединений потребовались представления о делокализованной ("групповой") ВАЛЕНТНОСТИ, характеризующей всю совокупность атомов С в ароматическом кольце.
Для теории ВАЛЕНТНОСТИ особый интерес представляют так называемые p-комплексы переходных металлов с ароматическими молекулами или молекулами с сопряжёнными связями в качестве лигандов (этиленом, циклопентадиенилом, бензолом и др.) типа ферроцена Fe (C5H5)2, дибензолхрома Cr(C6H6)2,тетрациклопентадиенила титана Ti (C5H5)4 и др. В отличие от комплексов типа [Сr (NHз)6]3+, [Сr (H2O)6]2+ или Cr (CO)6, где центральный атом осуществляет связь с лигандом через один атом от каждого лиганда (через N - в аммиакатах, через О - в гидратах, и т.д.), в p-комплексах атомы Fe, Cr и Ti взаимодействуют совершенно одинаково со всеми атомами С каждого ароматического кольца. Непригодность классической ВАЛЕНТНОСТИ здесь очевидна: при этом пришлось бы считать все атомы углерода 5-валентными, а атомы Fe, Cr и Ti - соответственно 10-, 12- и 20-валентными. Единственный неспаренный электрон, который имеется у радикала ×C5H5 (так же как и у многих других ароматических радикалов типа тропила ×C7H7 и т.д.), в равной степени принадлежит всем углеродным атомам кольца. Для этого класса соединений потребовались представления о делокализованной ("групповой") ВАЛЕНТНОСТИ, характеризующей всю совокупность атомов С в ароматическом кольце.
Сейчас стало ясно, что в комплексах, так же как ВАЛЕНТНОСТИ в простых соединениях, не является жестко специфической характеристикой элемента: для большого числа металлов были найдены комплексы со всеми промежуточными значениями КЧ от 3 до 7, 8 и 9. При этом возникли трудности с самим определением КЧ: в низкосимметричных высококоординационных комплексах расстояния М - Х, даже для одинаковых лигандов X, часто оказываются неодинаковыми; при этом они могут быть больше тех достаточно коротких расстояний, при которых наличие сильного взаимодействия бесспорно, но всё же недостаточно велики, чтобы их можно было уверенно исключить из координационной сферы комплекса.
Новые проблемы ВАЛЕНТНОСТИ возникли и в других разделах химии. Сильное развитие получила химия свободных радикалов [например, метил ×CH3, трифенилметил ×C (C6H5)3 и др., см., в которых имеются атомы 3-валентного углерода. В последнем десятилетии были синтезированы соединения инертных газов типа XeF2, XeF4, XeF6, XeO3 и др., то есть соединения элементов, которые ранее считались вообще неспособными к химическому взаимодействию. Стало ясно и то, что ВАЛЕНТНОСТЬ элементов может сильно меняться с изменением внешних условий, в частности температуры. Например, PCl5, существующий при умеренных температурах в газовой фазе в виде мономерных молекул, при конденсации диспропорционирует, давая пару катион [РСl4]+ (КЧ = 4) - анион [РСl6]- (КЧ = 6). Наоборот, при повышении температуры обнаруживаются молекулы PCl3, PCl2, PCl, ионы PCl4+, PCl3+, Pd2+, PCl+ и т.д. Благодаря успехам химии молекул в газовой фазе за последние 20 лет найдено огромное число соединений (часто сложного состава) с промежуточными и необычными ВАЛЕНТНОСТЯМИ, которые не обнаруживаются у соединений в обычных условиях. Например, кроме давно известных анионов типа CO32- и SO42-, сейчас обнаружены анионы CO3-, SO4- и нейтральные молекулы CO3, SO4. Кроме насыщенных молекул типа CH4, C2H6, найдены ионы типа CH5+, C2H7+, кроме молекулы H2 - ион Нз+, и т.д.
Сейчас установлено, что подавляющее большинство элементов может проявлять переменную ВАЛЕНТНОСТЬ, образуя весь ряд "валентноненасыщенных" соединений со всеми значениями ВАЛЕНТНОСТИ от 1 до максимальной с изменением на 1 (например, известны молекулы BF, BF2 и BF3; CF, CF2, CF3 и CF4 и т.д.). ВАЛЕНТНОСТЬ не может считаться жестко специфической характеристикой элемента, можно говорить лишь об относительной типичности или относительной устойчивости разных значений ВАЛЕНТНОСТИ. У непереходных элементов чётных и нечётных групп наиболее устойчивы соответственно чётные и нечётные ВАЛЕНТНОСТИ, например в молекулах типа PF3, PF5, SF2, SF4, SF6, IF, IF3, IF5, IF7 и т.д., где типичная ВАЛЕНТНОСТЬ атомов Р, S и I изменяется на 2 единицы.
