4. Уравнение состояния реального газа
Исследования показали, что уравнение Менделеева – Клапейрона не очень точно выполняется при исследовании разных газов. Голландский физик Я. Д. Ван-дер-Ваальс
первым понял причины этих отклонений: одна из них состоит в том, что вследствие огромного числа молекул, их собственный объем в целом сравним с объемом сосуда, в котором находится газ. С другой стороны, существование взаимодействия между молекулами газа слегка искажает показание манометров, с помощью которых обычно измеряют давление газа. В итоге Ван-дер-Ваальс
получил уравнение следующего вида: 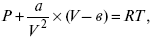
где а , в – постоянные величины для различных газов.
Недостаток этого уравнения в том, что а и в должны быть измерены для каждого газа эмпирически. Преимущество в том, что оно включает область перехода газа в жидкую фазу при высоких давлениях и низких температурах. Осознание этого сделало возможным получать любой газ в жидкой фазе.
Смотрите также
Классификация металлов и их сплавов
...
Диализ
...
Синтез этилового эфира 4-бромбенозойной кислоты
Цель работы состоит в
составление литературного обзора по спиртам и синтеза этилового эфира
4-бромбензойной кислоты.
Спиртами называются
органические вещества, молекулы которых содержат ...
