Векторная модель многоэлектронного атома
Микросостояния и атомные термы в приближении Рассела-Саундерса.
Этот раздел целесообразно рассмотреть на конкретных примерах.
Содержание. Электронная конфигурация. Микросостояния и их систематизация. Порядок учёта кулоновских взаимодействий и постадийная классификация дискретных электронных уровней и состояний атома (электронно-ядерное притяжение и орбитальные уровни, межэлектронное отталкивание и атомные термы Рассел-Саундерса, спиновая корреляция и запрет Паули). Суммарные квантовые числа ML,MS,L,S. Атомное внутреннее квантовое число J. Термы нормальные и обращённые. Правила Хунда (1-е, 2-е и 3-е). Относительная шкала энергии атомных термов. Спектральные переходы и правила отбора. Атомные уровни в магнитном поле, эффект Зеемана (практикум).
Электронная конфигурация представляет собой исходное понятие. Оно определяется в нулевом приближении в оценке энергии. Далее постепенно учитываются всё более тонкие взаимодействия, и возникает более точная картина состояний и уровней многоэлектронного атома. Если атомный подуровень заселён не полностью, то возникает несколько различных микросостояний. Их характеристики непосредственно определяются комбинаторикой размещений электронов в системе спин-орбиталей.
Если n электронов заселяют g спин-орбиталей, то одно из формальных обозначений конфигурации (g,n). В её пределах число возможных микросостояний определяется согласно статистике Ферми: W(g,n) = g!/[n! (g - n)!].
Пример 1: основная электронная конфигурация атома углерода C (1s22s22p2).
Конфигурация p2 (атомы IV группы элементов C, Si .). W(6,2) = 6! / [2! (6 -2) !]=15
|
Перечислим все возможные варианты орбитальных размещений и спиновых комбина-ций 2-х электронов на трёх АО: |
Орбитальные распределения двух электронов
|
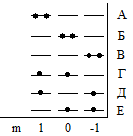
Возможно всего шесть размещений внутри p-АО без учёта спина Орбитальные распре-деления можно охарак-теризовать комбинаци-ями квантовых чисел частиц (m1, m2): (+1,+1) А ( 0, 0) Б ( -1, -1) В (+1, 0) Г ( +1, -1) Д ( 0, -1) Е |
Комбинации пространственных (орбитальных) состояний частиц в коллективе легко описать разными способами. Возможные спиновые комбинации в системе двух частиц-фермионов с половинным спином (электронов, протонов) можно представить разными способами. Можно изобразить ориентации спинов разными символами (стрелками, знаками или греческими буквами). Результат сложения компонент момента импульса вдоль оси вращения представим в одной из строк таблицы значениями суммарного магнитного квантового числа. Все возможные комбинации спиновых векторноотдельных электронов попадут в таблицу:
|
Способ 1 |
|
Ї |
Ї |
ЇЇ |
Эти три способа | ||||||
|
Способ 2 |
(++) |
(– +) |
(–+) |
(– –) |
Описания | ||||||
|
Способ 3 |
aa |
ab |
ba |
bb |
Идентичны | ||||||
|
Можно как-либо еще, а в итоге будет: |
где MS(1,2)= mS(1)+ mS(2) | ||||||||||
|
MS(1,2) |
1 |
0 |
0 |
-1 | |||||||
|
MS(1,2) |
+1 |
0 |
–1 | ||||||||
|
Микросостояния в рамке, выделенные на тёмном фоне, принципу Паули не удовлетворяют и должны быть исключены из дальнейшего анализа |
A |
А А |
А | ||||||||
|
A |
Б Б |
A | |||||||||
|
A |
В В |
A | |||||||||
|
Г |
Г |
Г |
Г | ||||||||
|
Д |
Д |
Д |
Д | ||||||||
Смотрите также
Расчет сметной стоимости проектируемого объекта
Капитальные
вложения в проектируемый объект принято называть полной сметной стоимостью
этого объекта. В проектных организациях расчет капитальных затрат
осуществляется путем составления локальных с ...
Химия сегодня
Химия - наука о веществах, изучающая их состав, строение,
свойства, а также превращения веществ, на сопровождающиеся изменением состава
атомных ядер.
"Широко простирает химия руки
с ...
Седьмая группа периодической системы
Из
членов данной группы водород был рассмотрен ранее. Непосредственно следующие за
ним элементы — F, Сl, Br и I — носят общее название г а л о г е н о в. К ним же
следует отнес ...