Дистиллированная вода
1
10
0
0,02
6.8
0.15
2
10
5
0,0133
10
0.1
3
10
10
0,01
12
0.083
4
10
15
0,008
16.9
0.059
5
10
20
0,0066
22
0.045
Расчет и анализ экспериментальных данных.
Уравнение реакции:
2KIO3+5Na2SO3+H2SO4=I2+5Na2SO4+K2SO4+H2O
или
2IO3-+5SO32-+2H+=I2+5SO42-+H2O
|
|
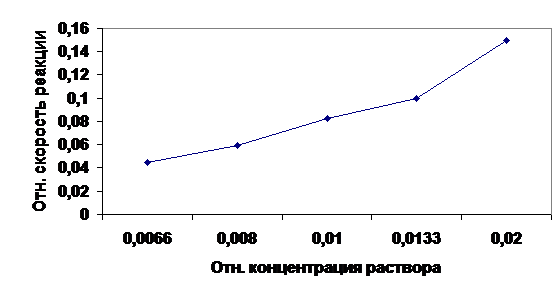
Рис1.График зависимости скорости протекания реакции от концентрации реагирующих веществ.
Выводы.
Из графика видно, что скорость является функцией концентрации реагирующих веществ. Это следует из того, что реагируют те молекулы, которые сталкиваются. Поэтому, чем больше концентрация (и следовательно вероятность столкновения молекул ) реагентов, тем выше скорость протекания реакции.
Смотрите также
Принципиальная схема проведения АЭСА
В основе спектрального
анализа лежит изучение строения света, который излучается или поглощается
анализируемым веществом. Рассмотрим схему эмиссионного спектрального анализа
(рис. 1). Для того чтоб ...
Возможная схема этапов оптимизации ХТС
Процессы
химической технологии это сложные физико-химические процессы, протекающие как в
пространстве, так и во времени. В них участвуют потоки энергии (тепло и холод)
и многофазные и много ...
Список
сокращений
1.
БЕ
– буферная емкость.
2.
БР
– блок подготовки и закачки реагента.
3.
БРХ
– блок реагентного хозяйства.
...