Загадочная вода
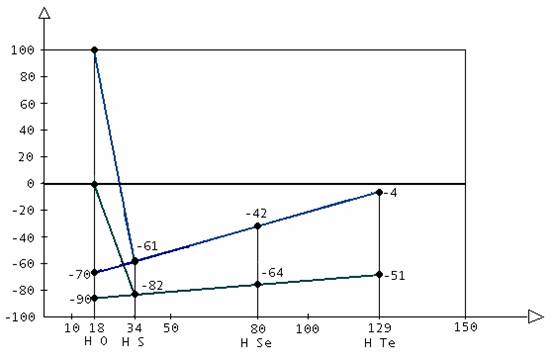 Если соединить нанесённые точки кипения Н2Те, Н2Sе, Н2S, получится почти прямая линия. Казалось бы, точка кипения воды должна лежать на её продолжении. Но она вдруг резко прыгает вверх, к 100°С. Та же странность происходит и при замерзании воды. По графику она должна была бы замерзнуть лишь при –90°С, между тем она превращается в лёд при 0°С.
Если соединить нанесённые точки кипения Н2Те, Н2Sе, Н2S, получится почти прямая линия. Казалось бы, точка кипения воды должна лежать на её продолжении. Но она вдруг резко прыгает вверх, к 100°С. Та же странность происходит и при замерзании воды. По графику она должна была бы замерзнуть лишь при –90°С, между тем она превращается в лёд при 0°С.
Разве может вода не подчинятся общим для других веществ физико-химическим законам? Значит, в мире молекул действуют какие-то неизвестные, а может быть, и не правильно понятые силы?
Объяснить, почему вода кипит при 100°С, а замерзает при 0°С, удалось лишь около 70 лет тому назад. Дело в том, что одна сторона их имеет положительный заряд, а другая – отрицательный. Про такие молекуле говорят, что они полярны. Полярность молекул вызвана тем, что атомы водорода присоединяются к атому кисло –рода не симметрично с боков, а в молекуле сероводорода или теллуристого водорода, а тяготеют к одной стороне.
Как только водород соединится с кислородом, тот час орбиты его электронов меняются, отклоняясь к кислороду. Ведь электроны водорода принадлежат теперь не ему одному, они стали общим достоянием водорода и кислорода. Но из-за изменения орбиты электронов ядра водорода, обладающие положительным зарядом, обнажаются. В целом молекула воды, конечно, остаётся нейтральной. Но та сторона её, где присоединился водород, оказывается положительной по заряду, а та, куда сдвинулись электроны, - отрицательна.
Из-за того, что молекулы воды полярны, между ними кроме обычных сил притяжения действуют ещё и электрические. Они получили названия водородных связей. Одна молекула воды может удержать ими возле себя целых 4 молекулы. Вот почему вода кипит не при –70°С, а при 100°С, и замерзает при температуре на 90° выше, чем ей полагалось бы.
Водородные связи делают воду чудесной, непохожей ни на какую другую, жидкость. Количество тепла, нужное для нагревания одного грамма её на один градус, иными словами теплоёмкость, в два раза больше, чем теплоёмкость спирта, в 30 – чем ртути. Способность воды запасать в себе, словно печка, большие количества тепла, а затем отдавать его обратно имеет огромное значение для жизни Земли. В тех местах, где её поблизости нет, разница между ночной и дневной температурами достигает 50°. При таком перепаде температур лопаются камни! В знойной Сахаре после испепе –ляющей жары, ночью без костра можно замёрзнуть! Оберегая растения от заморозков, садовники ставили в неотапливаемых оранжереях бочки с водой. Остывая на 10°, бочка давала столько же тепла, сколько небольшая охапка дров.
Для того чтобы нагреть 1 литр воды от 0° до 100°, надо затратить 100 кило калорий. Для того чтобы испарить тот же литр, - в 5 раз больше. Вот почему так холодно в мокром костюме. Удивительные свойства воды неисчислимы. Она вовсе не такая мягкая и под –датливая, как кажется. Об неё можно больно ушибится если неудачно нырнёшь. Столкновение дождинки с реактивным самолётом оставляет след на его корпусе. В США есть токарный станок, где вода режет бетон. Кажется невероятным, но вода прочна, как сталь.
Вода универсальный растворитель. В природе нет, ни одного вещества, которое бы не растворялось в тех или иных количествах. Тончайшие аналитические весы показали бы, что вместе со стаканом чая вы каждый день выпиваете 0,0001 грамма растворённого стекла.
Смотрите также
Белки, их строение и состав
БЕЛКИ — это азотсодержащие
высокомолекулярные органические вещества со сложным составом и строением молекул.
Белок можно
рассматривать как сложный полимер аминокислот.
Белки входят в
...
Атомно-кристаллическое строение металлов
...
Качественный анализ анионов
Цель аналитической химии - установление качественного и количественного
состава вещества или смеси веществ. В соответствии с этим аналитическая химия делится
на качественный и количественны ...
