Галогениды углерода.
-Cl
-Br
-I. Выше
-170
°С жидкий СF4 в любых соотношениях смешивается с жидким озоном (и может быть использован для его разбавления).
Диссоциация СF4 на фтор и имеющий пирамидальное строение трифторметильный радикал (СF3) требует затраты 581 кДж/моль. Известно очень много производных этого радикала. Обычно их получают при помощи СF3I (т. кип.
-22
°С), распад которого на I и CF3 протекает с очень небольшой энергией активации (8 кДж/моль).
МЕТАН.
В обычных условиях непосредственное взаимодействие углерода (аморфного) и водорода с образованием метана (СН4) по реакции
С + 2 Н2
Û СН4 + 75 кДж
практически не происходит. При нагревании и в присутствии катализатора (мелкораздробленный Ni) устанавливается равновесие, положение которого сильно зависит от температуры (рис. 8). Помимо этого синтетического пути, метан может быть получен рядом других методов из более сложных соединений углерода. В природе он постоянно образуется при разложении органических веществ без доступа воздуха (например, в болотах). Он часто содержится в природных газах и обычно входит в состав искусственно получаемого светильного газа.
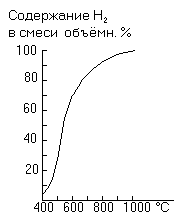
Рис. 8. Равновесие синтеза метана.
Метан является простейшим представителем многочисленных соединений углерода с водородом, называемых углеводородами и изучаемых в органической химии. Сам он представляет собой бесцветный и не имеющий запаха газ, малорастворимый в воде. С химической стороны метан характеризуется своей большой инертностью, на него не действуют ни щёлочи, ни кислоты. С кислородом он в обычных условиях не реагирует, но при поджигании сгорает по реакции:
СН4 + 2 О2 = СО2 + 2 Н2О.
Горение метана сопровождается очень большим выделением тепла (803 кДж/моль).
Метан является основой атмосфер тяжёлых планет (Юпитера, Сатурна). Следы его (1,4
·10-4 объёмн. %) всегда содержатся в земной атмосфере. Интересно, что повышение содержания метана привлекает комаров.
Большие количества метана (часто свыше 90%) содержат многие скопившиеся в подземных пустотах природные газы. Такие газы являются очень хорошим топливом, 1 м3 которого даёт при сгорании 33
-38 тыс. кДж. Вместе с тем они служат основным сырьём для промышленного получения водорода. Обычно применяемый при этом метод основывается на неполном окислении метана по уравнению:
2 СН4 + О2 = 2 СО + 4 Н2 + 71 кДж.
Получаемый газ подвергается затем вторичной обработке водяным паром.
На территории СНГ известны многочисленные месторождения богатых метаном природных газов (Саратов, Ставрополь, Бухара и др.). Благодаря высокой калорийности и удобству транспортировки (по трубопроводам), такой газ с каждым годом занимает всё более важное место в общем топливном балансе страны.
Горение смеси метана (и других горючих газов) с воздухом идёт только в том случае, если процентный состав смеси не выходит из некоторых определённых границ. Так, пределы воспламеняемости (в процентах горючего газа по объёму) составляют 5
-15 для метана, 12
Смотрите также
Синтез пиррольных интермедиатов для высокосопряженных порфиринов
...
Расчет фонда заработной платы работающих .
Расчет
фонда заработной платы предполагает определение годового фонда и средней
заработной платы отдельных категорий и групп работающих. ...
