Цвет полярных молекул
Когда катионы попадают в поле действия анионов, то возникает взаимное влияние (рис. 10). Результаты зависят от способности электронных оболочек ионов к деформации. Эта способность обусловлена природой иона и силой, с которой данный ион может воздействовать на оболочки соседей. Как правило, ионы малого радиуса и большого положительного заряда деформируются слабо: очень крепко в таком случае положительное ядро притягивает электроны. Деформируемость и связанная с ней поляризация невелика и в том случае, если внешняя электронная оболочка иона подобна оболочке инертного газа, т. е. завершено ее заполнение электронами.
Если молекула состоит из ионов с заполненными электронными оболочками (MgO, ZnS), то возможность перехода электрона практически исключена, так как ему, попросту говоря, некуда переходить. Тогда из всего спектра видимого света молекула не отдает предпочтения ни одному участку. Такие молекулы не имеют окраски. В растворе они бесцветны, а в твердом состоянии белые. К такому типу красящих веществ относятся оксид цинка, оксид магния, фосфат и сульфид цинка, сульфат бария. Как видите, это все соединения элементов II группы периодической системы с полностью завершенными внутренними электронными оболочками.
Подобные соединения прямо могут служить неорганическими красителями — пигментами. В качестве красителей используются такие индивидуальные соединения, как, например, белила — оксид цинка или оксид титана (IV); чернь — это одно из аллотропных состояний углерода — сажа. Цвет может появиться лишь в том случае, если катион с подуровнями, заполненными электронами, связан с анионом, способным к значительной поляризации, например с тяжелыми ионами галогенов, таких, как Вг- или I-, некоторыми кислородсодержащими анионами PO43-, AsO43- и целым рядом других. Соли и оксиды металлов, имеющих атомы с незаполненными оболочками, в большинстве своем обладают окраской. Ионы металла имеют примерно тот же цвет, который присущ им в водном растворе: Си2+ — голубой, Сг3+ — зеленый и т. п. Существуют многочисленные анионы, способные придавать окраску ионам, особенно если это ионы металлов побочных подгрупп. Так, например, желтый анион CrO42- влияет на бесцветный катион серебра Ag+, что в результате реакции:
2Ag+ + CrO42- → Ag2CrO4
образуется красный осадок хромата серебра. В подобной же реакции бесцветный ион ртути Hg2+ образует оранжевое соединение HgCrO4. Однако, ион свинца — металла главной подгруппы IV группы, соединяясь с CrO42-, так и оставляет желтым цвет хромата свинца РbСгO4.
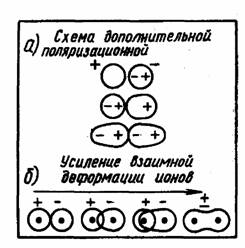
Рис. 10. Возникновение поляризационного эффекта (а) и усиление (б) взаимной деформации ионов.
Взаимное влияние катионов и анионов позволяет варьировать оттенки цвета.
Поэтому чаще всего применяются соединения переменного состава: желтый крон — смесь хрома и сульфата свинца РbСгO4 • nРbSO4, изумрудная зелень - гидроксид хрома переменного состава Сг203 • nН2O (n= 1,5—2,5), кобальт светло-фиолетовый и фиолетовый — фосфаты кобальта, гидратированные водой Соз(РО4)2 • 8Н2О или СоNH4PО4.
Таким образом, окраска полярной молекулы зависит от наличия у катиона свободных электронных подуровней, от способности катиона поляризовать анион и соответственно от способности этого аниона к поляризации.
Смотрите также
Синтез 1,1-дихлор-2-метил-2-фенилциклопропана
...
Выводы по проекту
Эффективный фонд времени работы оборудования составил
8426,4 ч./год.
Капитальные затраты на здания и оборудование составляют 81931,5 тыс. руб.
Средняя годовая заработная плата одного основного
...
