Экспериментальная часть. Синтез тетрахлорида олова.
|
Вещество |
Молярная масса, М г/моль |
Масса m, г |
Кол-во вещества, ν моль |
Физические константы | ||
|
mтеор |
mпракт |
νтеор |
νпракт | |||
|
Олово |
119 |
38,84 |
38,84 |
0,326 |
0,326 | |
|
Оксид марганца (IV) |
87 |
56,72 |
150 |
0,652 |
1,72 | |
|
Соляная кислота |
36,5 |
95,19 |
473,2 |
2,61 |
ω = 36,5% ρ = 1,183г/мл | |
MnO2 + 4HCl = MnCl2 + Cl2↑ + 2H2O
Sn + 2Cl2 = SnCl4
Собрать прибор (рис. 6) и тщательно высушить его.
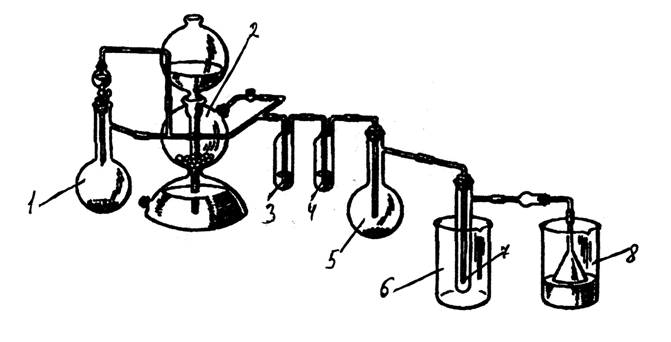
Рис 6. Прибор для получения хлорида олова (IV).
В колбу Вюрца емкостью 500 мл (1) засыпали оксид марганца (IV), в капельную воронку залили концентрированную соляную кислоту. В аппарат Киппа (2) засыпали мрамор (карбонат кальция), залили соляную кислоту. В реакционную колбу на 25 мл (5) засыпали металлическое олово. В промывалку (3) налили дистиллированную воду, в промывалку (4) – 96%-ю серную кислоту. В химический стакан (6) засыпали лёд. Хлоркальциевую трубку заполнили хлоридом кальция, воронку опустили в стакан со щёлочью (8).
Открыв кран на аппарате Киппа, продували прибор углекислым газом около 15 мин:
CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
Прекратив подачу CO2, открыли капельную воронку, начали нагревать колбу (1):
MnO2 + 4HCl = MnCl2 + Cl2↑ + 2H2O
Когда колба (5) заполнится хлором, начали нагревать её.
Sn + 2Cl2 = SnCl4
Олово начало гореть жёлто-белым пламенем. Нагрев возобновляли только в случае замедления реакции. По окончании реакции пробирка (7) заполнилась жёлтой жидкостью – хлоридом олова (IV).
Выход:
m(SnCl4)практ = 18,49 г
ν(SnCl4)теор = ν(Sn) = 0,326 моль
m(SnCl4)теор = ν(SnCl4)*M(SnCl4) = 0,326*261 = 85,09 г
ω = ![]() =
= ![]() =
= ![]()
Смотрите также
Энтропия органических веществ при нормальных и повышенных давлениях
...
Современные и перспективные требования и технологии к качеству
тяжелых моторных и судового маловязкого топлива
Настоящие
технические условия распространяются на топливо маловязкое судовое получаемое
из дистиллятных фракций прямой перегонки и вторичной переработки нефти.
Топливо
маловязкое судов ...
