Методы синтеза.
На основании приведённых данных можно выделить следующие методы синтеза хлорида олова (IV):
Первый способ
.
Удобный способ получения безводного SnCl4 основан на прямом синтезе:
Sn + 2Cl2 = SnCl4
Большую пробирку (длина 20—25 см, диаметр 3—4 см) заполняют на 3/4 гранулированным оловом. Пробирку закрывают пробкой с двумя отверстиями: в одно вставляют газоподводящую трубку, а другое — форштосс обратного холодильника (рис.3).
|
|
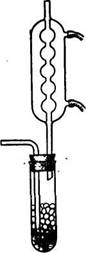
Рис. 3. Прибор для получения хлорного олова
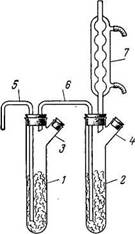
Рис. 4. «Сдвоенный» прибор для получения хлорного олова:
1,2 — пробирки; 3,4 — тубусы; 5 — хлорподводящая трубка; 6 — соединительная трубка; 7—шариковый холодильник.
В пробирку наливают несколько миллилитров готового SnCl4 и пропускают (под тягой) сухой хлор с такой скоростью, чтобы газ успевал прореагировать с оловом. Реакция протекает бурно, иногда с появлением пламени. Когда на дне пробирки соберется значительный слой SnCl4, газоподводящую трубку несколько поднимают, но конец ее должен быть погружен в жидкость. По окончании реакции SnCl4 сливают в склянку, вносят несколько гранул Sn для связывания свободного хлора и выдерживают 1 ч в закрытой склянке. Затем жидкость перегоняют, собирая фракцию, кипящую при 112—114 oС (приемник для предохранения от влаги воздуха снабжают хлоркальциевой трубкой). Если исходное олово содержало Fe, то перегонку SnCl4 не следует доводить до конца (во избежание перехода примеси FeCl3). Полученный препарат переливают в склянку со стеклянной или корковой (но не резиновой!) пробкой.
Для приготовления большого количества SnCl4 (до 3 кг в день) рекомендуется прибор, изображенный на рис. 4. Две пробирки 1 и 2 (длина 20—25 см, диаметр 4 см) с тубусами 3 и 4 соединяют трубкой 6. К пробирке 2 присоединяют обратный холодильник 7. Пробирки заполняют на 3/4 гранулированным оловом и по трубке 5 пропускают ток сухого хлора, сначала медленно, во избежание сильного разогревания, затем, когда трубка 5 окажется погруженной в SnCl4, быстрее.
Когда пробирка 1 почти заполнится SnCl4 (пробирка 2 к этому времени наполняется приблизительно до половины) ток хлора прекращают, под трубку 5 подставляют сухую склянку и через верхнее отверстие холодильника 7 с помощью резиновой груши в прибор подают струю воздуха. При этом SnCl4 почти полностью переливается в подставленную склянку. Затем пробирки снова заполняют через тубусы оловом и продолжают хлорирование. Для очистки препарат перегоняют, добавив немного листового олова для связывания растворённого хлора. Собирают фракцию, кипящую при 112-114 оС.
Выход 90-95%. [5]
Второй способ.
Собирают прибор согласно схеме (рис. 4.22).
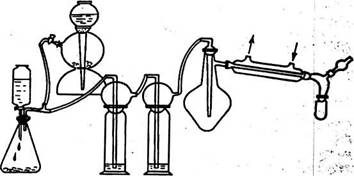
Рис. 5. Прибор для получение хлорида олова (IV).
Все части прибора должны быть тщательно высушены . В реакционную колбу помещают определенное количество металлического олова, заполняют прибор углекислым газом, колбу нагревают до плавления олова и пропускают в нее ток сухого очищенного хлора. Дальнейшее нагревание продолжают в том случае, если реакция замедляется.
Sn + 2Cl2 = SnCl4
По окончании реакции из системы вытесняют хлор сухим углекислым газом. Выход продукта оценивают по объему и плотности полученного вещества. Часть хлорида олова (IV) отгоняют в пробирку с оттянутым концом, которую затем запаивают, или в пробирку которую закрывают пробкой и парафинируют. Оставшуюся часть продукта используют для изучения его свойств.
Третий способ.
Безводный препарат можно получить также хлорированием безводного SnCl2
SnCl2 + Cl2 = SnCl4
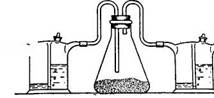
Рис. 6. Прибор для получения хлорного олова из SnCl2
В коническую колбу (рис. 5) помещают 200 г безводного SnCl2 и пропускают (под тягой) струю хлора со скоростью 60—70 пузырьков в минуту. Хлор предварительно пропускают через склянку Тищенко с конц. H2SO4. Избыток хлора поглощается в другой склянке Тищенко с раствором NaOH. Реакция протекает с сильным разогреванием реакционной смеси (до 70—80 оС) и вскоре кристаллическая масса SnCl2 превращается в жидкость (SnCl4). Конец реакции определяется по постепенному снижению температуры. Полученную жидкость переливают в колбу для перегонки, добавляют немного листового олова для связывания растворенного хлора и медленно перегоняют, собирая фракцию, кипящую при 112—114 оС.
Выход 250 г (90%).
На основании анализа литературных данных и исходя из наших возможностей, для получения тетрахлорида олова использовали метод, основанный на непосредственном взаимодействии олова с хлором (второй способ).
Смотрите также
Свойства и получение хлорида кальция
...
Организация производства
В
данном разделе рассматривается организация производственного процесса на
проектируемом объекте, описывается режим работы этого объекта и рассчитывается
эффективный фонд времени работы ведущего об ...
Электрохимические процессы на границе. Твердый электролит. Соединения внедрения
...