Хлорид кальция. Физико-химические свойства
Хлорид кальция СаСІ2 образует белые кристаллы кубической формы с плотностью 2,51 г/см3. Плавится при 772°С. Сильно гигроскопичен, на воздухе расплывается. Равновесная относительная влажность воздуха над СаСІ2 ×2Н2О при 20°С равна 22%, при 50°С – 17%, а над СаС12×6Н2О при 10°С – 38%, при 20°С – 32,3%, при 24,5°С – 31%. Высушивание гранулированным хлоридом кальция при 25°С позволяет понизить влажность газа до 0,14 – 0,25 г воды в 1 л.
С аммиаком СаСІ2 образует двойные соединения CaCl2×4NH3. СаСІ2×8NH3.
При повышенных температурах СаС12 разлагается кислородом воздуха и парами воды по реакциям
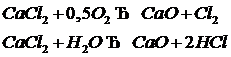
а в присутствии SiO2 или ![]() идут реакции:
идут реакции:
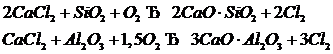
Заметное разложение СаС12 в сухом и влажном воздухе идет выше 830°С, в присутствии ![]() – выше 720°С, в присутствии Al2O3 выше 800°С.
– выше 720°С, в присутствии Al2O3 выше 800°С.
Известен субхлорид кальция СаС12 устойчивый при температуре выше 800°С, образующийся при нагревании СаС12 с металлическим кальцием. Субхлорид кальция окрашен в красно-фиолетовый цвет. Он может быть получен при комнатной температуре в метастабильном состоянии при быстром переохлаждении.
В солянокислых растворах растворимость СаС12 уменьшается и тем в большей степени, чем ниже температура. При 0° в растворе с содержанием 27,98% НС1 растворяется 9,1% СаС12 (вместо 37,30% в воде), при 15°С и содержании в растворе 26,20% НС1 растворяется 21,3% СаС12 (вместо 41,2% в воде). В системе НС1—СаС12—Н2О при 15°С кристаллизуются две твердые фазы: СаС12×2Н2О и СаС12×6Н2О, при 25°С – три твердые фазы: СаС12×2Н2О, СаС12×4Н2О, СаС12×6Н2О. Хлорид кальция высаливает NaCl из его водных растворов, особенно при пониженных температурах. Растворимость NaCI в системе СаС12—NaCl—Н2О (при 0°С) непрерывно уменьшается по мере растворения СаС12 (от 26,23% в воде до 0,62% в растворе, содержащем 34,87% СаС12). При более высоких температурах, помимо NaCl, кристаллизуются также СаС12.
Смотрите также
Полигалогенпроизводные алканов
...
Введение
Цель
практического эмиссионного спектрального анализа состоит в качественном
обнаружении, в полуколичественном или точном количественном определении
элементов в анализируемом веществе. В зависимост ...
Структура процесса обслуживания официантами
Метод обслуживания официантами применяется в ресторанах, кафе и закусочных первой и высшей категории, а также в некоторых столовых. Структура процесса обслуживания официантами состоит из двух стадий: ...
