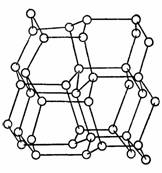
Аллотропные видоизменения углерода.
|
Рис.1 Модель решетки алмаза.
|
Углерод существует в трех аллотропных модификациях: алмаз, графит и карбин.
Две основные разновидности углерода - графит и алмаз - существенно отличаются по свойствам. Мягкий графит имеет слоистое строение (рис. 2).Все атомы углерода находятся здесь в состоянии sp2-гибридизации: каждый из них образует три ковалентные связи с соседними атомами, причем углы между направлениями связи равны 120°. Графит электропроводен и хорошо раскалывается по плоскости. В обычных условиях графит и является наиболее устойчивой модификацией. Переход графита в алмаз возможен при очень высоких давлениях (порядка 125000 атм) и температурах (около 3000 °С). Однако исследование этого процесса сначала с теоретических позиций, а затем экспериментальным путем показало, что в присутствии катализаторов (железо, платина) графит превращается в алмаз уже при давлении 60000—80000 атм и температуре 1400—1600 °С. В настоящее время налажено производство искусственных алмазов для технических целей, причем размеры их обычно колеблются от 0,5 до 4 мм; в отдельных случаях удается получить и большие экземпляры. Структура алмаза (рис. 1) типично тетраэдрическая; атомы углерода прочно соединены за счет перекрытия sp3-орбиталей. Хотя в обычных условиях алмаз нестабилен, но практически он может сохраняться неопределенно долгое время. При сильном накаливании алмаза происходит его постепенная графитизация.
Смотрите также
Материальный баланс
Схему переработки можно разбить на 5 блоков:
Дробление и измельчение.
Грануляция и окисление в печи кипящего слоя.
Выщелачивание и фильтрация.
Осаждение и фильтрация.
Прокалка и су ...
Синтезы органических соединений на основе оксида углерода
Помимо синтезов органических соединений из СО и Н2
– углеводороды, олефины, в том числе изобутилен с высокими показателями
(селективность > 90%), спирты, в том числе изобутанол с выходом ...