Химические связи
Различают несколько типов химических связей: 1 – ионная. Ионная связь образуется при взаимодействии атомов, которые сильно различаются по электроотрицательности (связь между типичным металлом и типичным неметаллом).

Na0-1e = Na+ Cl0+1e = Cl—
Ионная связь характерна также для щелочей и солей, в которые входят кислород и активные металлы.
2 – ковалентная связь образуется при перекрывании электронных облаков.
Ковалентная неполярная образуется при взаимодействии атомов с одинаковыми электроотрицательностями.
![]()
Ковалентная полярная образуется при взаимодействии атомов, электроотрицательности которых различаются незначительно.
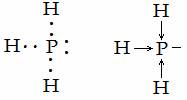
3 – металлическая связь образуется во всех металлах. Это связь, которую осуществляют относительно свободные электроны с положительными ионами металлов в кристаллической решётке. Атомы металла легко отдают валентные электроны и превращаются в положительные ионы. Относительно свободные электроны перемещаются между положительными ионами металла и между ними возникает металлическая связь, то есть электроны как бы цементируют положительные ионы металла в кристаллической решётке.
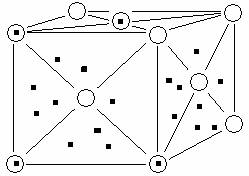
4 – водородная связь – это связь между атомом водорода одной молекулы и атомом сильного электроотрицательного элемента другой молекулы.
Водородная связь – это молекулярная связь. Она слабее, чем ионная и ковалентная связь.
Смотрите также
Влияние вязкости и дисперсности несовместимых полимеров на волокнообразование в их смесях
В настоящее время широкое применение получают методы формования
полимерных материалов с заданной структурой на основе смесей несовместимых
полимеров. Так, кристаллизующиеся полимеры при соде ...
Вода
Вода, у тебя нет ни цвета, ни вкуса, ни запаха, тебя
невозможно описать, тобой наслаждаются, не ведая, что ты такое. Нельзя сказать,
что необходимо для жизни: ты сама жизнь. Ты исполняешь ...
Ядерная энергетика
Атомная энергетика - область техники,
основанная на использовании реакции деления атомных ядер для выработки теплоты
и производства электроэнергии. В 1990 атомными электростанциями (АЭС) ми ...
