Изменение энтропии в различных процессах.
![]() , причем знак = относится к обратимым процессам, а знак > к необратимым.
, причем знак = относится к обратимым процессам, а знак > к необратимым.
Если требуется вычислить энтропию необратимого процесса необходимо провести обратимый процесс между теми же самыми конечным и начальным состоянием (используем тот факт, что энтропия – функция состояния).
а) Изотермический процесс:
![]() , Q – часто это скрытая теплота фазовых переходов.
, Q – часто это скрытая теплота фазовых переходов.
б) Изменение температуры при ![]()
![]() :
:
![]()
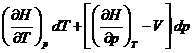 , следовательно
, следовательно 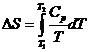 , т.к.
, т.к. ![]()
Энтропия необратимого процесса: ![]()
Теплота конденсации при 298 К равна – 10519 кал, ![]()
Ответ, очевидно, неверен, поскольку процесс необратимый. Проведем его обратимо: ![]()
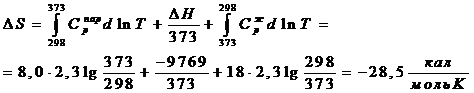
(-9769 – теплота конденсации при 373 К)
![]()
Заметим, что действительно ![]() меньше, чем
меньше, чем ![]() .
.
4.5. Закон Джоуля
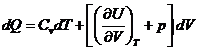 ,
,
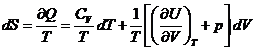 – это полный дифференциал, следовательно
– это полный дифференциал, следовательно 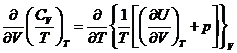 .
.
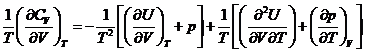 ,
, ![]()
![]()
![]() .
.
Для идеального газа ![]()
![]() и
и ![]() ,
,
Для любых систем ![]() ,
,
Для газа Ван-дер-Ваальса ![]() и
и ![]() .
.
Смотрите также
Химия запахов
Почти 2000 лет назад античный учёный, поэт
и философ Тит Лукреций Кар полагал, что в носовой полости есть крошечные поры
разных размера и формы. Каждое пахучее вещество,
рассуждал он, испус ...
Введение
Физическая химия – наука, объясняющая химические
явления и устанавливающая их закономерности на основе общих принципов физики.
Общая задача физической химии – предсказание
временного хода химичес ...
Производство метанола
Метанол (метиловый
спирт) является одним из важнейших по значению и масштабам производства
органическим продуктом, выпускаемым химической промышленностью. Впервые метанол
был найден в древ ...
