Термохимия. Энтальпия.
Если система характеризуется только одним внешним параметром V, т.е. может совершаться только работа расширения, тогда первый закон может быть записан в виде: ![]() .
.
Если ![]() т.е. тепловой процесс эффекта равен изменению функции состояния. Найдем такую функцию состояния, изменение которой равно тепловому эффекту при постоянном давлении. Для этого выражение для I закона необходимо преобразовать так, чтобы давление находилось под знаком дифференциала. Обратим внимание, что
т.е. тепловой процесс эффекта равен изменению функции состояния. Найдем такую функцию состояния, изменение которой равно тепловому эффекту при постоянном давлении. Для этого выражение для I закона необходимо преобразовать так, чтобы давление находилось под знаком дифференциала. Обратим внимание, что
d(pV) = pdV + Vdp и pdV = = d(pV) – Vdp, а подстановка в выражение для I закона дает:
dQ = dU + d(pV) – Vdp = d(U + pV) – Vdp = dH -Vdp
|
H ≡ U + pV |
– функция состояния называется энтальпией. |
![]() . При
. При ![]()
![]() .
.
Выберем в качестве независимых переменных Т и р, тогда:
![]()
![]()
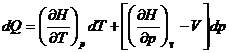
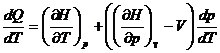
![]() – отношение приращения независимых переменных является неопределенной величиной, чтобы избежать этого нужно указать конкретный процесс. Если p = Const, то
– отношение приращения независимых переменных является неопределенной величиной, чтобы избежать этого нужно указать конкретный процесс. Если p = Const, то ![]()
Очевидно, есть определенная симметрия между U и H:
![]()
Смотрите также
Синтез м-нитробензальдегида
Данная
исследовательская работа проведена для получения м-нитробензальдегида и
подробного изучения свойств альдегидов, которые широко используются в промышленности, в органическом
синтезе и ...
Плотность жидкости при нормальной температуре кипения
...
Идеи алхимии
Алхимия
(позднелат. alchemia, alchimia, alchymia) - своеобразное явление культуры,
особенно широко распространённое в Западной Европе в эпоху позднего
средневековья. Слово «алхимия» произво ...
