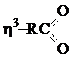Правило сохранения 16-18 электронной оболочки Толмена в элементарных стадиях
Уже давно было отмечено (Сиджвик, 1929), что в стабильных комплексных соединениях общее количество электронов вокруг атома металла равно числу электронов ближайшего инертного газа. Это число электронов было названо эффективным атомным номером (ЭАН). В случае d-металлов число электронов в валентной оболочке металла, связанного с лигандами, должно быть равно 18 (d10s2p6). Такая оболочка и считается устойчивой. Например, Ni(CO)4: Ni0 d10, CO – 2-х электронный лиганд. Следовательно, 10 + 8 = 18. Для расчета числа электронов в комплексе металла необходимо сложить число электронов в валентной оболочке атома металла (или иона) и число электронов, предоставляемых нейтральными лигандами (или анионами). Для этого используют ковалентнуюи ионную
модели химической связи. В первом случае комплекс включает ионы Mn+, X– и нейтральные лиганды L, а во втором – атомы металла, нейтральные группы X (гомолитический разрыв связи M–X) и нейтральные лиганды L. Например, в комплексе HMn(CO)5 в валентной оболочке Mn имеем для ионной модели:
H– (2 эл) + Mn+ (6 эл) + 5CO (10 эл) = 18 эл.
для ковалентной модели:
H· (1 эл) + Mn0 (7 эл) + 5CO (10 эл) = 18 эл.
В таблице 2.1 приведены некоторые лиганды, их обозначения и количества электронов, предоставляемых металлу в рамках ковалентной и ионной моделей.
Таблица 2.1
|
Лиганды |
Символ лиганда |
Ковалентная модель |
Ионная модель |
|
Me, Ph, H, Cl, OH, CN |
X |
1 эл |
2 эл |
|
CO, NH3, H2O, PR3, R2S |
L |
2 эл |
2 эл |
|
C2H4 |
L |
2 эл |
2 эл |
|
H2 |
L |
2 эл |
2 эл |
|
|
LX |
3 эл |
4 эл |
|
h3–C3H5 |
LX |
3 эл |
4 эл |
|
h3–C5H5 |
L2X |
5 эл |
6 эл |
|
h3–C6H6 |
L3 |
6 эл |
6 эл |
В координационной химии достаточно много исключений из правила 18 электронной оболочки (в основном, в случае металлоорганических комплексов): Ni(C5H5)2 – 20 электронов, W(CH3)6 – 12 электронов. Тем не менее обобщение большого экспериментального материала позволило Толмену сформулировать следующее правило:
интермедиаты, образующиеся в реакциях комплексных и металлоорганических соединений, обычно имеют 18- или 16-электронные оболочки. Именно такие интермедиаты существуют в заметных количествах.
Таким образом, в стадиях с участием d-металлов, которые рассматриваются как элементарные, число валентных электронов должно меняться на 2 единицы (18®16®18 и т.д.). Комплексы, имеющие в валентной оболочке 16 электронов, естественно, более реакционноспособны в реакциях замещения лигандов, поскольку в этом случае возможен ассоциативный механизм замещения:
![]()
Например, Rh(acac)(C2H4)2 (16 эл) обменивает этилен (13C2H4) по ассоциативному механизму с константой скорости ³ 104 сек–1 (25оС, Р = 1 атм), а (C5H5)Rh(C2H4)2 (18 эл) обменивает этилен по диссоциативному механизму с константой скорости ~ 4×10–10 сек–1.
Из трех вариантов механизма внедрения молекулы СО по связи СН3–Mn вариант (1) согласно правилу Толмена наименее вероятен:
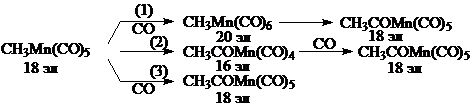
Смотрите также
Производство метанола
Метанол (метиловый
спирт) является одним из важнейших по значению и масштабам производства
органическим продуктом, выпускаемым химической промышленностью. Впервые метанол
был найден в древ ...
Синтез метанола
...
Сложные реакции
...