Влияние поверхностного потенциала воды на реологические свойства дисперсных систем
Дисперсные системы относятся к гетерогенным системам и состоят из двух и более фаз [1]. Одна из фаз является сплошной и называется дисперсионной средой. Другие фазы раздроблены и распределены в первой; они называются дисперсными фазами. Дисперсные системы, в которых дисперсионной средой является вода, широко распространены в природе и играют важную роль в технике (кровь живых организмов, грязевые потоки, суспензии в производстве керамики и т.д.). Реологические свойства этих дисперсных систем в значительной степени зависят от свойств межфазной границы «вода - дисперсная фаза». Поэтому исследование этих зависимостей весьма актуально при решении ряда задач по регулированию свойств дисперсных систем.
При погружении частиц дисперсной фазы в водную среду происходит специфическая адсорбция всегда присутствующих в воде ионов Н3О+ и OH- на поверхность. Величины адсорбции ионов Н3О+ и OH- обусловлены особенностям химического состава, кристаллической структуры и состояния поверхности частиц дисперсной фазы. Свойства межфазных границ «вода – дисперсная фаза» зависят также от поверхностного потенциала воды. Известно, что в нейтральной среде поверхность воды имеет отрицательный потенциал -450 мВ, несмотря на то, что концентрация ионов [Н3О+] равна концентрации ионов [OH-] [2]. Ионы OH- по своему строению сильнее отличаются от строения молекул воды, чем ионы Н3О+, что и объясняет их повышенную поверхностную активность (рис.1). Поэтому, как правило, поверхность частиц в дисперсных системах заряжается отрицательно, что способствует снижению вязкости дисперсных систем благодаря уменьшению сил межчастичного трения в результате действия кулоновских сил взаимного отталкивания между частицами.
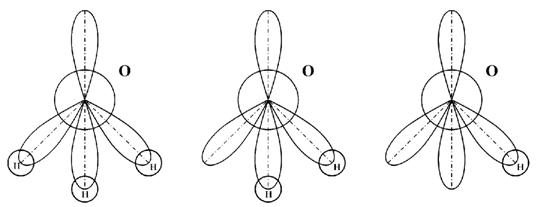
Рис.1. Схема строения иона Н3О+ , молекулы воды и иона OH-
Соотношение ионов Н3О+ и OH-, адсорбирующихся на поверхности воды, и, следовательно, потенциал поверхности воды, зависят от исходного соотношения ионов Н3О+ и OH- в воде, т.е. от кислотности (рН) водной среды. Это подтверждается данными, приведенными на рис.2. Потенциал поверхности дистиллированной воды определяли по методике, описанной в работе [2]. Для изменения рН использовались водные растворы HCl и NaOH. Увеличение рН (щелочная среда) вызывает увеличение доли адсорбированных ионов OH- и, соответственно усиливает отрицательный заряд на поверхности воды. В кислой среде происходит снижение и последующая инверсия поверхностного потенциала. Величину рН, соответствующую нулевому потенциалу поверхности воды (5,4), назовем точкой нулевого заряда (ТНЗ).
В технике часто приходится решать задачу получения стабильных концентрированных дисперсных систем (суспензий, шликеров) с низкой вязкостью. Это важно при операциях транспортировки дисперсных систем по трубопроводам, измельчения, сушки, формования и т.д. При этом необходимо предотвратить налипание дисперсных систем на стенки трубопроводов, реакторов и рабочие поверхности технологического оборудования. Похожие задачи встречаются и в медицине, например, снижения вязкости крови при высоком содержании эритроцитов и предотвращения формирования атеросклеротических бляшек на стенках кровеносных сосудов.
Известно, что кровь человека и других живых организмов имеет щелочную реакцию. Отрицательный поверхностный потенциал поверхности воды обеспечивает формирование отрицательного потенциала на стенках кровеносных сосудов и поверхности эритроцитов. В результате снижается вязкость крови и вероятность формирования атеросклеротических бляшек на стенках кровеносных сосудов из-за возрастания кулоновских сил отталкивания между отрицательно заряженными поверхностями. Аналогичные явления наблюдаются и в суспензиях керамических порошков. Как видно из данных, приведенных на рис.3, налипание суспензий Fe2O3 на поверхности пластин стали и оргстекла происходит в кислой и нейтральной средах. В основной среде налипания не происходит, а имеет место даже “растворение” налипшей массы и очистка пластин. В щелочной среде повышается седиментационная устойчивость суспензии и снижается вязкость.
Смотрите также
Железо и его роль
Герою знаменитого романа
Даниэля Дефо повезло. Корабль, с которого он спасся, сидел на мели совсем
недалеко от острова. Робинзон сумел погрузить на плот все необходимое и
благополучно переп ...
Ассортимент, качество и состав тяжелых видов моторных топлив
Стандарт на котельное
топливо — ГОСТ 10585—75 предусматривает выпуск четырех его марок: флотских
мазутов Ф-5 и Ф-12, которые по вязкости классифицируются как легкие топлива,
топочных мазу ...
Электролиз
...
