2. Уравнение изотермы химической реакции
Если реакция протекает обратимо, то ΔG = 0.
Если реакция протекает необратимо, то ΔG ≤ 0 и можно рассчитать изменение ΔG. 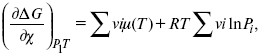
где χ – пробег реакции – величина, которая показывает, сколько молей изменилось в ходе реакции. I сп – характеризует равновесное и неравновесное состояние реакции, II сп – характеризует только неравновесные состояния.
Если
д χ = 1,
то 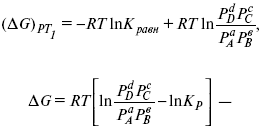
это уравнение изотермы химической реакции
. 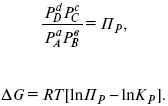
С помощью уравнения изотермы химической реакции можно судить о направлении протекания реакции.
1) Пp< Кp, ΔG < 0, слева направо;
2) Пp> Кp, ΔG > 0, справа налево;
3) Пp= Кp, ΔG = 0, химическое равновесие.
Смотрите также
Вывод
В процессе производственной деятельности
образуются отходы, которые нарушают экологическое равновесие, загрязняя
окружающую среду, и снижают степень извлечения ценных компонентов, содержащихся
в ис ...
Водородная связь
Помимо различных
гетерополярных и гомеополярных связей, существует еще один особый вид связи,
который в последние два десятилетия привлекает все большее внимание химиков.
Это так называемая ...
Расчет фонда заработной платы работающих .
Расчет
фонда заработной платы предполагает определение годового фонда и средней
заработной платы отдельных категорий и групп работающих. ...
